Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Định luật bảo toàn khối lượng và phương trình hóa học SVIP
1. Định luật bảo toàn khối lượng
➤ Thực hiện thí nghiệm tìm hiểu về sự bảo toàn khối lượng
Dụng cụ và hoá chất: cân điện tử, đũa thủy tinh, 2 cốc thủy tinh, dung dịch barium chloride (BaCl2) và dung dịch sodium sulfate (Na2SO4).
Bước 1: Lấy 30 mL mỗi dung dịch trên cho vào lần lượt 2 cốc thủy tinh có đánh số (1) và (2).
Bước 2: Đem cân 2 cốc thủy tinh chứa 2 dung dịch, ghi nhận giá trị khối lượng.
Bước 3: Rót dung dịch trong cốc (1) vào cốc (2) rồi dùng đũa thủy tinh khuấy nhẹ cốc (2) cho hai dung dịch trộn lẫn vào nhau. Quan sát hiện tượng.
Bước 4: Đặt lại 2 cốc trên cân và ghi nhận giá trị khối lượng đo được.


Định luật bảo toàn khối lượng:
"Trong một phản ứng hoá học, tổng khối lượng của các chất sản phẩm bằng tổng khối lượng các chất tham gia phản ứng."
2. Phương trình hoá học
➤ Tìm hiểu phương trình hóa học
Trong các phản ứng hóa học, chất tham gia phản ứng ở bên trái mũi tên (→) chỉ chiều phản ứng và chất sản phẩm ở bên phải mũi tên (→).
Sơ đồ tổng quát của một phản ứng:
Chất phản ứng → Sản phẩm
Để thuận tiện cho việc trình bày ngắn gọn một phản ứng hóa học, người ta sử dụng các công thức hóa học biểu diễn cho các chất, gọi là phương trình hóa học.
Khi chuyển từ sơ đồ phản ứng thành phương trình hóa học, ta cần chú ý:
- Viết đúng công thức hóa học cho tất cả các chất.
- Sắp xếp theo đúng vị trí công thức hóa học của chất phản ứng và sản phẩm.
- Liên kết các công thức hóa học bằng dấu + và kí hiệu → để được một phương trình hóa học hoàn chỉnh.
Ví dụ 1: Phản ứng giữa đinh sắt (iron, Fe) và dung dịch sulfuric acid (H2SO4) tạo ra iron(II) sulfate (FeSO4) và khí hydrogen (H2).
Ta biểu diễn thành sơ đồ phản ứng dạng chữ như sau:
Iron + Sulfuric acid → Iron(II) sulfate + Hydrogen
Thay tên các chất bằng công thức hóa học, được sơ đồ phản ứng:
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
➤ Thực hiện các bước lập phương trình hóa học
Một phương trình hóa học được xem là cân bằng khi nó thỏa mãn định luật bảo toàn khối lượng (tức là số nguyên tử của mỗi nguyên tố ở hai vế phương trình phải bằng nhau).
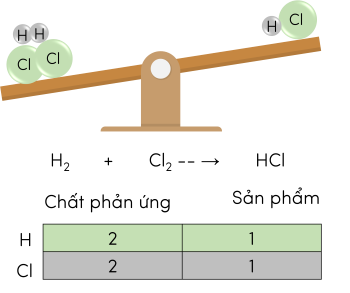
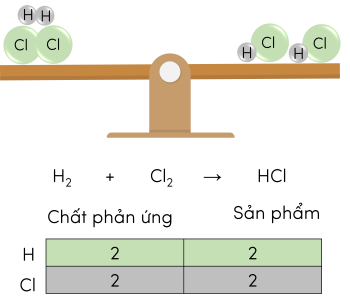
Để lập phương trình hóa học hay còn gọi là cân bằng số nguyên tử của các chất trong phản ứng, ta tiến hành theo 3 bước.
Ví dụ 2: Biết phosphorus tác dụng với khí oxygen tạo ra diphosphorus pentoxide (P2O5). Hãy lập phương trình hóa học của phản ứng.
| Bước 1: Viết sơ đồ phản ứng | \(P+O_2--\rightarrow P_2O_5\) |
| Bước 2: Cân bằng số nguyên tử của mỗi nguyên tố |
Ta làm chẵn số nguyên tử O về phía phải bằng cách đặt hệ số 2 trước P2O5: \(P+O_2--\rightarrow\) \(2\)\(P_2O\)\(_5\) Để số nguyên tử O về trái bằng với về phải, ta thêm hệ số 5: \(P\) \(+\) \(5\)\(O\)\(_2\)\(--\rightarrow\) \(2\)\(P_2O\)\(_5\) Số nguyên tử P về trái và phải chưa bằng nhau, ta đặt hệ số 4 trước P: \(4\)\(P+5O_2\rightarrow\) \(2\)\(P\)\(_2\)\(O_5\) |
| Bước 3: Viết phương trình hóa học hoàn chỉnh | \(4P+5O_2\rightarrow2P_2O_5\) |
Lưu ý:
- Khi cân bằng không được thay đổi chỉ số trong những công thức hóa học đã viết đúng.
- Nếu trong công thức hóa học có nhóm nguyên tử (ví dụ nhóm (OH), nhóm (SO4),…), ta xem cả nhóm như một đơn vị để cân bằng.
Ví dụ 3:
\(Mg\left(NO_3\right)_2+2KOH\rightarrow Mg\left(OH\right)_2\downarrow+2KNO_3\)
➤ Tìm hiểu ý nghĩa của phương trình hoá học
Phương trình hóa học cho biết tỉ lệ về số nguyên tử hoặc số phân tử giữa các chất trong phản ứng. Tỉ lệ này bằng đúng với tỉ lệ hệ số mỗi chất trong phương trình.
Ví dụ 4: Theo phương trình hóa học có tỉ lệ chung:
| \(4\)\(P\) | \(+\) | \(5\)\(O_2\) | \(\rightarrow\) | \(2\)\(P_2O_5\) |
| 4 nguyên tử P | : | 5 phân tử O2 | : | 2 phân tử P2O5 |
Nghĩa là cứ 4 nguyên tử P tác dụng với 5 phân tử O2, tạo ra 2 phân tử P2O5.
1. Định luật bảo toàn khối lượng: "Trong một phản ứng hoá học, tổng khối lượng của các chất sản phẩm bằng tổng khối lượng các chất tham gia phản ứng".
2. Phương trình hóa học biểu diễn phản ứng hóa học bằng công thức hóa học của các chất tham gia và chất sản phẩm.
3. Phương trình hóa học cho biết tỉ lệ về số nguyên tử hoặc số phân tử giữa các chất trong phản ứng.
Ba bước để lập phương trình hóa học:
- Viết sơ đồ phản ứng.
- Cân bằng số nguyên tử của mỗi nguyên tố.
- Viết phương trình hóa học hoàn chỉnh.

Bạn có thể đánh giá bài học này ở đây