Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Lý thuyết SVIP
I. KHÁI NIỆM, DANH PHÁP
1. Khái niệm
- Khi thay thế nhóm -OH của axit cacboxylic RCOOH bằng nhóm OR' thì ta thu được hợp chất hữu cơ mới có công thức RCOOR' được gọi là este.
- Số lượng nhóm -COO- chính là số chức của este, nó phụ thuộc vào số chức của axit và ancol.
- Este đơn chức là este được tạo bởi axit cacboxylic đơn chức RCOOH và ancol đơn chức R'OH và có công thức chung là RCOOR'.
- Este được tạo thành từ axit no, đơn chức, mạch hở và ancol no, đơn chức, mạch hở được gọi là este no, đơn chức, mạch hở có công thức phân tử là CnH2nO2 (với n ≥ 2).
2. Danh pháp
| Tên của este RCOOR’: tên gốc R’ + tên gốc axit RCOO thay đuôi ‘ic’ bằng ‘at’. |
Một số gốc đặc biệt:
| Công thức cấu tạo | Tên gọi |
| -CH=CH2 | Vinyl |
| CH2=CH-COO- | acryl |
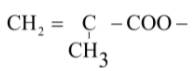 | meta acryl |
Ví dụ:
| Công thức cấu tạo | Tên gọi |
| CH3COOCH3 | Metyl axetat |
| C2H5COOCH3 | Metyl propionat |
| CH3COOCH=CH2 | Vinyl axetat |
| CH2=CHCOOC2H5 | Etyl acrylat |
II. TÍNH CHẤT VẬT LÍ
- Là chất lỏng hoặc rắn ở điều kiện thường.
- Rất ít tan trong nước.
- Nhiệt độ sôi, nhiệt độ nóng chảy thấp hơn so với ancol và axit tương ứng có cùng số cacbon vì este không tạo được liên kết hidro liên phân tử với nhau và khả năng tạo liên kết hidro với nước của este cũng rất kém khiến chúng rất ít tan trong nước.
- Các este thường có mùi thơm đặc trưng.
| Este | Mùi este | Ảnh minh họa |
Etyl fomat | Đào chín | |
Isoamyl axetat | Chuối chín |  |
Benzyl axetat | Hoa nhài |  |
| Etyl butirat n-C3H7COOC2H5 | Dứa chín |  |
III. TÍNH CHẤT HÓA HỌC
Tính chất hóa học đặc trưng của este là phản ứng thủy phân. Este bị thủy phân trong cả môi trường axit hoặc bazơ.
1. Thủy phân trong môi trường axit (phản ứng thuận nghịch)
Phương trình tổng quát:
RCOOR' + H2O ![]() RCOOH + R'OH
RCOOH + R'OH
Ví dụ:
C2H5COOCH3 + H2O ![]() C2H5COOH + CH3OH
C2H5COOH + CH3OH
Chú ý: Các este không no có dạng RCOO-CH=CH-R' hoặc RCOO-C(R')=CH-R'' khi bị thủy phân trong môi trường axit tạo thành axit cacboxylic và andehit hoặc xeton.
Ví dụ:
CH3COOCH=CH2 + H2O ![]() CH3COOH + CH2=CH-OH (không bền)
CH3COOH + CH2=CH-OH (không bền)
CH2=CH-OH (không bền) ➜ CH3CHO (bền)
Vậy phương trình hóa học của phản ứng thủy phân vinyl axetat CH3COOCH=CH2 trong môi trường axit là:
CH3COOCH=CH2 + H2O ![]() CH3COOH + CH3CHO (andehit axetic)
CH3COOH + CH3CHO (andehit axetic)
2. Thủy phân trong môi trường kiềm (phản ứng một chiều)
Phương trình tổng quát:
RCOOR' + NaOH → RCOONa + R'OH
Chú ý: Tương tự phản ứng thủy phân trong môi trường axit, các este không no có dạng RCOO-CH=CH-R' hoặc RCOO-C(R')=CH-R'' khi bị thủy phân trong môi trường kiềm tạo thành muối của axit cacboxylic và andehit hoặc xeton.
Ví dụ:
CH3COOC(CH3)=CH2 + H2O → CH3COONa + (CH3)2CO (axeton)
3. Phản ứng của gốc hidrocacbon
Các este không no có thể tham gia phản ứng cộng với dung dịch brom, cộng hidro tương tự như cộng vào anken, ankin. Ví dụ:
CH3COOCH=CH2 + Br2 (dd) → CH3COOCH(Br)-CH2Br
Các este có gốc HCOO- có khả năng tham gia phản ứng tráng gương tượng tự andehit.
IV. ĐIỀU CHẾ
Các este thường được điều chế bằng cách đun sôi hỗn hợp gồm ancol và axit cacboxylic, có xúc tác là H2SO4 (phản ứng este hóa).
RCO-OH + H-OR' ![]() RCO-OR' + H2O
RCO-OR' + H2O
Axit H2SO4 vừa là chất xúc tác cho phản ứng điều chế, vừa có tác dụng hút nước làm cân bằng chuyển dịch theo chiều thuận, tăng hiệu suất phản ứng.
Tuy nhiên, có một số este không điều chế được bằng phương pháp này mà phải điều chế bằng phương pháp riêng. Ví dụ:
Vinyl axetat CH3COOCH=CH2 được điều chế bằng phản ứng cộng giữa axit axetic và axetilen.
CH3COOH + CH\(\equiv\)CH \(\underrightarrow{t^o,xt}\) CH3COOCH=CH2
V. ỨNG DỤNG
- Dùng làm dung môi để tách, chiết chất hữu cơ, pha sơn.
- Một số polime của este đùng để sản xuất chất dẻo như poli(vinyl axetat), poli(metyl metacrylat) dùng làm thủy tinh hữu cơ,...
- Một số este có mùi hương không độc, dùng làm chất tạo hương trong công nghiệp thực phẩm, mĩ phẩm...

Trong quá trình học tập, nếu có bất kỳ thắc mắc nào, các em hãy để lại câu hỏi ở mục hỏi đáp để cùng thảo luận và trả lời nhé. Chúc các em học tốt!


Bạn có thể đánh giá bài học này ở đây