Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Sự chuyển thể của các chất SVIP
I. SƠ LƯỢC CẤU TRÚC CỦA CHẤT RẮN, CHẤT LỎNG, CHẤT KHÍ
1. Mô hình động học phân tử
Để mô tả cấu trúc và giải thích một số tính chất của chất rắn, chất lỏng, chất khí người ta sử dụng một mô hình được gọi là mô hình động học phân tử. Mô hình này được xây dựng dựa trên các giả thuyết sau:
- Các chất được cấu tạo từ các hạt riêng biệt là phân tử.
- Các phân tử chuyển động không ngừng. Chuyển động của các phân tử được gọi là chuyển động nhiệt.
- Các phân tử chuyển động càng nhanh thì nhiệt độ của vật do chúng tạo nên càng cao.
- Giữa các phân tử có lực hút và đẩy gọi chung là lực liên kết phân tử.
Với mô hình động học phân tử, sự khác biệt về độ lớn của lực tương tác giữa các phân tử trong các thể dẫn đến sự khác biệt về cấu trúc của chất rắn, chất lỏng và chất khí.
2. Sơ lược cấu trúc của chất rắn
Trong chất rắn, các phân tử ở rất gần nhau.
 - Copy.jpg)
Lực tương tác
- Lực tương tác giữa các phân tử chất rắn rất mạnh nên giữ được các phân tử ở các vị trí cân bằng và mỗi phân tử chỉ có thể dao động xung quanh vị trí cân bằng xác định này. Do đó, các chất ở thể rắn có thể tích và hình dạng xác định.
Phân loại
- Chất rắn kết tinh (hay chất rắn tinh thể) có cấu trúc tinh thể, tạo bởi các hạt (nguyên tử, phân tử, ion) liên kết chặt với nhau và sắp xếp theo một trật tự hình học xác định, tuần hoàn trong không gian gọi là mạng tinh thể. VD: muối ăn, kim cương,...
- Chất rắn vô định hình không có cấu trúc tinh thể. VD: thủy tinh, nhựa đường, cao su,...
3. Sơ lược cấu trúc của chất lỏng
Trong chất lỏng, các phân tử ở xa nhau hơn so với các phân tử trong chất rắn.
 - Copy - Copy.jpg)
Lực tương tác
- Lực tương tác gữa các phân tử chất lỏng nhỏ hơn trong chất rắn nên không giữ được các phân tử ở vị trí xác định nhưng vẫn đủ để giữ các phân tử không chuyển động phân tán xa nhau.
- Các phân tử chất lỏng linh động hơn các phân tử chất rắn do chúng dao động xung quanh các vị trí cân bằng và các vị trí cân bằng này lại có thể dịch chuyển. Vì vậy, chất lỏng có thể tích xác định nhưng không có hình dạng riêng mà có hình dạng của phần bình chứa nó.
4. Sơ lược cấu trúc của chất khí
Trong chất khí, các phân tử ở xa nhau hơn so với các phân tử trong chất lỏng.

Lực tương tác
- Khoảng cách giữa các phân tử rất lớn so với kích thước của chúng nên lực tương tác giữa các phân tử hầu như không đáng kể (trừ khi va chạm nhau).
- Các phân tử chất khí chuyển động hỗn loạn, không ngừng về mọi phía, chiếm toàn bộ không gian của bình chứa. Vì vậy, chất khí không có thể tích và hình dạng riêng mà có thể tích và hình dạng của bình chứa.
II. SỰ CHUYỂN THỂ
1. Sự chuyển thể của chất
Các chất có thể chuyển từ thể này sang thể khác.
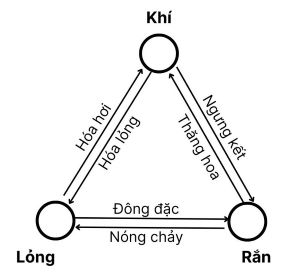
- Quá trình chuyển từ thể rắn sang thể lỏng của các chất được gọi là sự nóng chảy. Quá trình chuyển ngược lại, từ thể lỏng sang thể rắn được gọi là sự đông đặc.
- Quá trình chuyển từ thể lỏng sang thể khí (hơi) của các chất được gọi là sự hóa hơi (bao gồm bay hơi và sôi). Quá trình chuyển ngược lại, từ thể khí (hơi) sang thể lỏng được gọi là sự ngưng tụ (sự hóa lỏng).
2. Giải thích sự nóng chảy
Ở trạng thái rắn, phân tử của chất kết tinh được xếp chặt và có thứ tự trong lưới tinh thể. Các liên kết giữa các phân tử tạo ra một cấu trúc vững chắc và cứng. Khi nhiệt độ tăng các phân tử nhận thêm năng lượng từ môi trường. Khi nhiệt độ đạt đến giá trị nóng chảy, năng lượng đủ lớn để phân tử vượt qua liên kết giữa chúng, chúng có thể tự do chuyển động trong không gian trở thành các phân tử ở thể lỏng.

3. Giải thích sự hóa hơi
Sự hoá hơi có thể xảy ra dưới hai hình thức là bay hơi và sôi.
Sự bay hơi là sự hoá hơi xảy ra ở mặt thoáng của chất lỏng. Một số phân tử tại đây có động năng đủ lớn để thắng lực liên kết của các phân tử chất lỏng khác, thoát được ra khỏi mặt thoáng của chất lỏng trở thành các phân tử ở thể hơi.
Sự sôi là sự hoá hơi xảy ra đồng thời ở bên trong và trên mặt thoáng của chất lỏng. Khi nhiệt độ của nước tăng tới khoảng 100 oC thì nước bắt đầu sôi. Khi đó các bọt chứa không khí và hơi nước nổi lên trong lòng nước càng ngày càng tăng, tới mặt thoáng thì vỡ, không khí và hơi nước thoát ra ngoài khí quyển trở thành các phân tử ở thể hơi.

| Chất | Nhiệt độ nóng chảy (oC) | Nhiệt độ sôi (oC) |
|
Tungsten (wolfram) |
3422 | 5555 |
| Đồng | 1300 | 2580 |
| Chì | 327 | 1 749 |
| Thủy ngân | -39 | 357 |
| Rượu | -117 | 80 |
1. Trong chất rắn, các phân tử ở gần nhau, lực tương tác mạnh và mỗi phân tử dao động xung quanh vị trí cân bằng xác định.
2. Trong chất lỏng, khoảng cách giữa các phân tử xa hơn so với trong chất rắn, lực tương tác yếu hơn so với trong chất rắn và các phân tử dao động xung quanh các vị trí cân bằng có thể di chuyển được.
3. Trong chất khí, khoảng cách giữa các phân tử rất lớn, lực tương tác giữa các phân tử không đáng kể nên các phân tử chuyển động hỗn loạn, không ngừng.
4. Khi nóng chảy, các phân tử chất rắn nhận năng lượng sẽ phá vỡ liên kết với một số phân tử xung quanh và trở nên linh động hơn, chất rắn chuyển thành chất lỏng.
5. Khi hóa hơi, các phân tử chất lỏng nhận được năng lượng sẽ tách khỏi liên kết với các phân tử khác, thoát khỏi khối chất lỏng và chuyển động tự do. Chất lỏng chuyển thành chất khí.

Bạn có thể đánh giá bài học này ở đây