Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Tính chất hóa học của carbohydrate SVIP
I. Tính chất hóa học của glucose và fructose
Glucose và fructose đều thể hiện tính chất của alcohol đa chức và của hợp chất carbonyl.
1. Phản ứng với copper(III) hydroxide
Thí nghiệm 1: Phản ứng của glucose với copper(II) hydroxide
Bước 1: Thêm 2 mL dung dịch NaOH 10% 0,5 mL vào dung dịch CuSO4 5%.
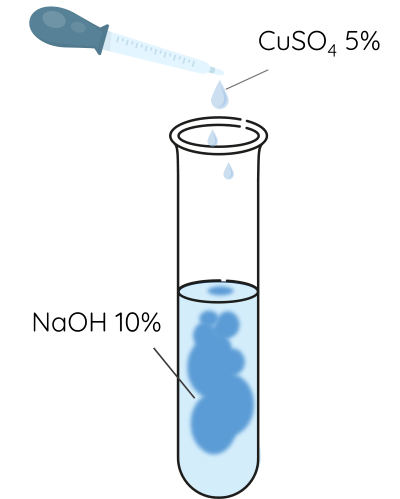
Bước 2: Thêm tiếp vào ống nghiệm 3 mL dung dịch glucose 2% vào ống nghiệm và lắc đều.
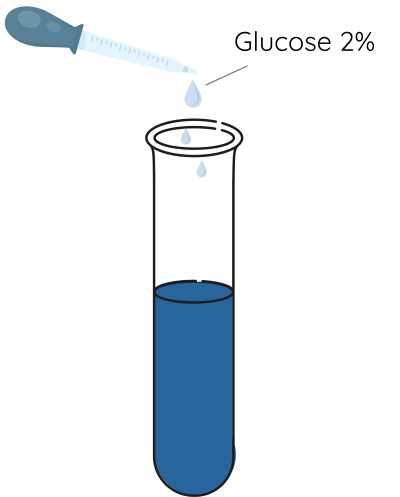
Bước 3: Đun nhẹ đến khi ống nghiệm đổi màu hoàn toàn.
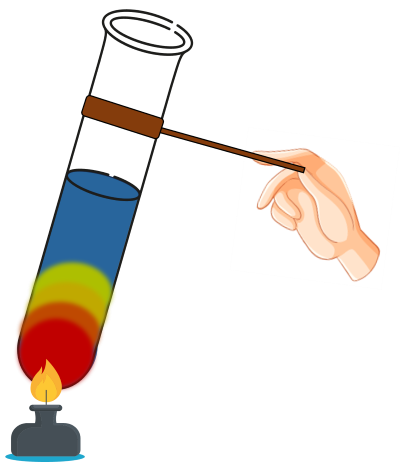
Glucose và fructose tác dụng với copper(II) hydroxide trong môi trường kiềm ở điều kiện thường tạo thành phức chất màu xanh lam, tan trong nước.
2C6H12O6 + Cu(OH)2 → Cu(C6H12O6)2 + 2H2O
Đun nóng dung dịch chứa glucose và Cu(OH)2 trong môi trường kiềm sẽ xuất hiện kết tủa màu đỏ gạch do Cu(OH)2 bị khử thành Cu2O. Đây là tính chất của nhóm chức aldehyde trong phân tử glucose.
\(CH_2OH\left[CHOH\right]_4CHO+2Cu\left(OH\right)_2+NaOH\overset{t^o}{\rightarrow}CH_2OH\left[CHOH\right]_4COONa+Cu_2O+3H_2O\)
Fructose cũng tham gia phản ứng như trên và tạo thành kết tủa đỏ gạch Cu2O tương tự như glucose do trong môi trường kiềm, fructose có thể chuyển hóa thành hợp chất có nhóm chức aldehyde:
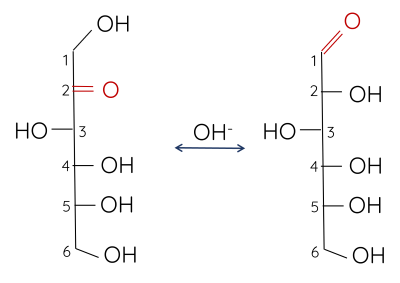
2. Phản ứng với thuốc thử Tollens
Thí nghiệm 2: Phản ứng của glucose với thuốc thử Tollens
Bước 1: Thêm từ từ dung dịch NH3 5% vào 2 mL dung dịch AgNO3 1%. Lắc đến khi kết tủa tan hết.
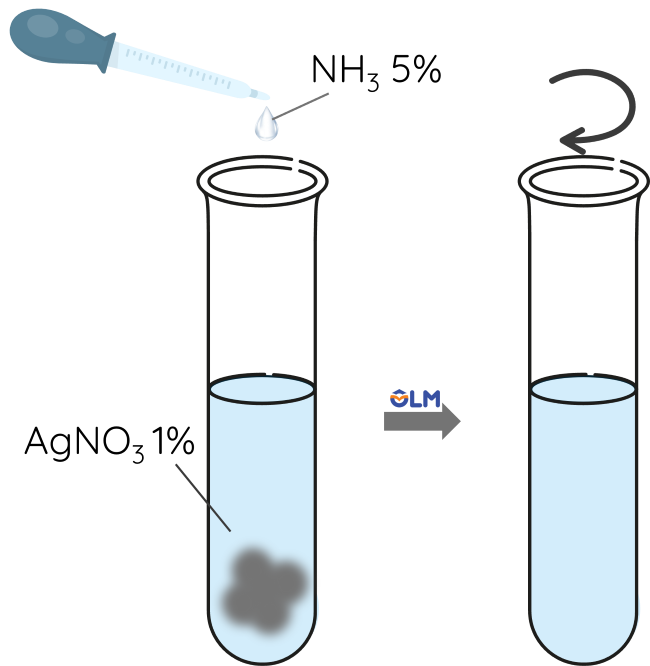
Bước 2: Thêm 2 mL dung dịch glucose 2%, lắc đều.
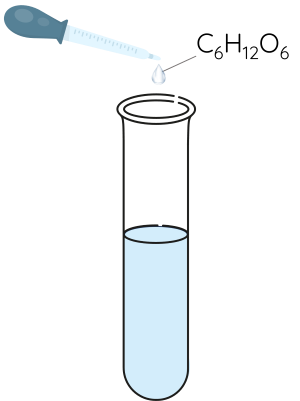
Bước 3: Ngâm ống nghiệm vào cốc thủy tinh chứa nước nóng và chờ trong vài phút.
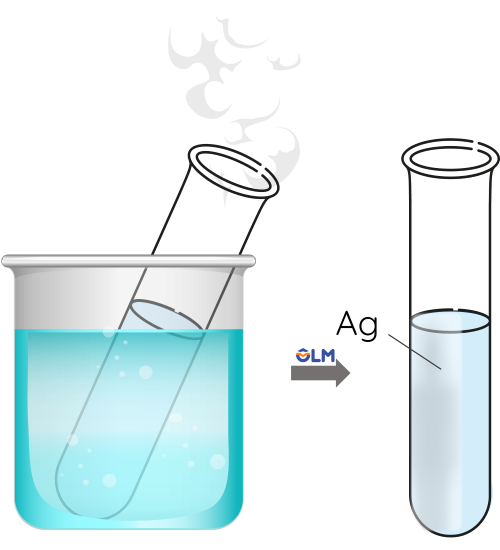
Glucose và fructose đều tham gia phản ứng với thuốc thử Tollens để tạo thành kết tủa bạc kim loại (phản ứng tráng bạc).
Ví dụ 1:
\(CH_2OH\left[CHOH\right]_4CHO+2\left[Ag\left(NH_3\right)_2\right]OH\overset{t^o}{\rightarrow}CH_2OH\left[CHOH\right]_4COONH_4+2Ag+3NH_3+H_2O\)
3. Phản ứng với nước bromine
Thí nghiệm 3: Phản ứng của glucose với nước bromine
Cho khoảng 1 mL nước bromine loãng vào ống nghiệm. Sau đó, thêm từ từ 2 mL dung dịch glucose 2%, lắc đều.

Phản ứng của glucose với nước bromine làm nước bromine bị mất màu và tạo thành gluconic acid theo phương trình hóa học sau:
\(CH_2OH\left[CHOH\right]_4CHO+Br_2+H_2O\rightarrow CH_2OH\left[CHOH\right]_4COOH+2HBr\)
Fructose không làm mất nước màu bromine.
4. Phản ứng với alcohol
Khi dẫn khí hydrogen chloride và dung dịch của glucose trong alcohol, nhóm -OH hemiacetal được thay thế bằng -OR của alcohol.

5. Phản ứng lên men
Glucose và fructose bị lên men tạo thành các sản phẩm khác nhau, tùy thuộc và loại enzyme có trong men được sử dụng.
Ví dụ 2:
Lên men rượu:
\(C_6H_{12}O_6\overset{enzyme}{\rightarrow}2C_2H_5OH+2CO_2\)
II. Tính chất hóa học của saccharose
Saccharose có những tính chất của một alcohol đa chức. Ngoài ra, saccharose thuộc loại disaccharide có thể tham gia phản ứng thủy phân để tạo thành các monosaccharide.
1. Phản ứng với copper(III) hydroxide
Thí nghiệm 4: Phản ứng của saccharose và copper(II) hydroxide.
Bước 1: Cho khoảng 0,5 mL dung dịch CuSO4 5% vào ống nghiệm chứa 2 mL dung dịch NaOH 10%.
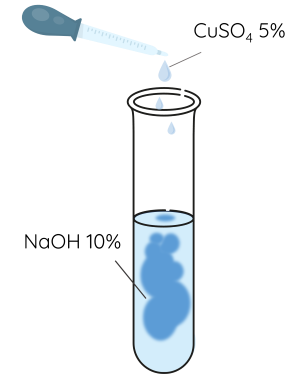
Bước 2: Cho khoảng 3 mL dung dịch saccharose 5% vào ống nghiệm, lắc đều.
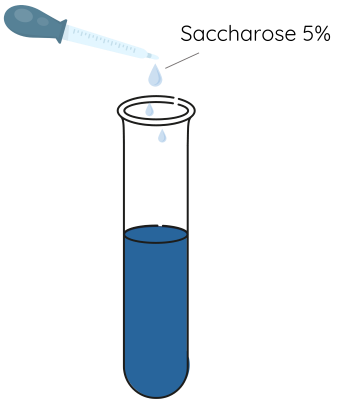
Bước 3: Đun nóng nhẹ ống nghiệm
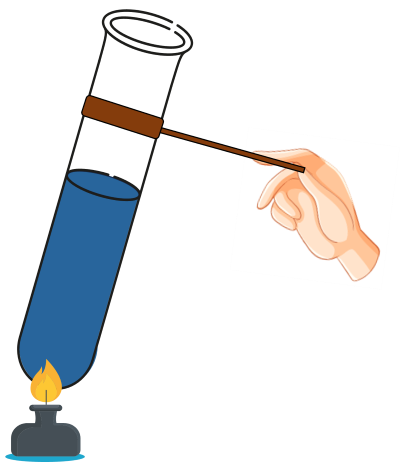
Dung dịch màu xanh lam được tạo thành khi cho dung dịch saccharose tác dụng với copper(II) hydroxide trong môi trường kiềm.
2C12H22O11 + Cu(OH)2 → Cu(C12H21O11)2 + 2H2O
2. Phản ứng thủy phân
Saccharose bị thủy phân tạo thành glucose và fructose. phản ứng xảy ra khi có xúc tác acid hoặc có mặt của enzyme.
\(C_{12}H_{22}O_{11}+H_2O\overset{H^+,t^o}{\rightarrow}C_6H_{12}O_6\left(Glu\right)+C_6H_{12}O_6\left(Fruc\right)\)
III. Tính chất hóa học của tinh bột
1. Phản ứng với iodine
Thí nghiệm 5: Phản ứng tạo màu giữa tinh bột và iodine
Cho vài giọt iodine trong KI vào ống nghiệm chứa 1 mL dung dịch hồ tinh bột

Phân tử tinh bột hấp thụ iodine tạo thành hợp chất có màu xanh tím. Quá trình này được dùng để nhận ra tinh bột bằng iodine và ngược lại.
2. Phản ứng thủy phân
Thí nghiệm 6: Phản ứng thủy phân tinh bột
Bước 1: Cho khoảng 1 mL dung dịch H2SO4 1M vào ống nghiệm chứa 2 mL dung dịch hồ tinh bột.
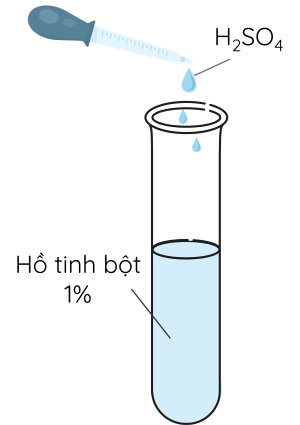
Bước 2: Đặt ống nghiệm vào cốc nước nóng và đun cách thủy. Sau khoảng 20 phút thì lấy ra, cho thêm vài giọt dung dịch I2. Nếu dung dịch có màu vàng thì ngừng đun, nếu dung dịch đun tiếp và tiếp tục thử màu.

Bước 3: Thêm từ từ NaOH đến khi dung dịch chuyển sang môi trường kiềm (thử bằng quỳ tím).
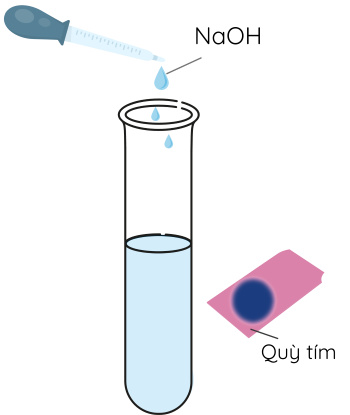
Bước 4: Cho khoảng 2 mL dung dịch thu được vào ống nghiệm chứa 0,5 mL dung dịch NaOH và 1 mL dung dịch CuSO4.
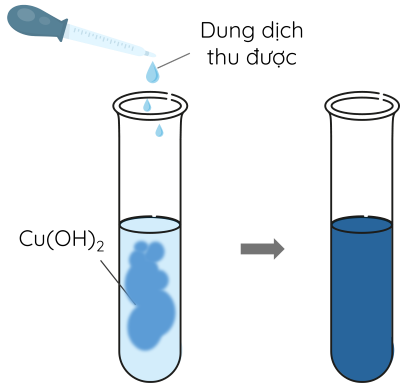
Bước 5: Đun nóng nhẹ ống nghiệm đến khi thay đổi màu sắc kết tủa.
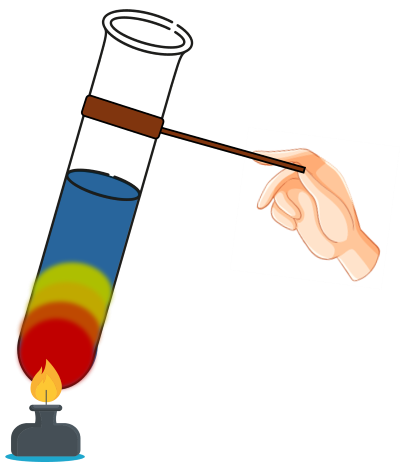
Phản ứng thủy phân tinh bột xảy ra khi có xúc tác acid (hoặc enzyme) và diễn ra quá nhiều giai đoạn. Các giai đoạn trung gian tạo thành dextrin (C6H10O5)x (với x < n) và maltose. Sản phẩm cuối cùng của quá trình thủy phân là glucose.
\(\left(C_6H_{10}O_5\right)_n+nH_2O\overset{H^+,t^o}{\rightarrow}nC_6H_{12}O_6\)
IV. Tính chất hóa học của cellulose
1. Phản ứng thủy phân
Thí nghiệm 7. Phản ứng thủy phân cellulose
Bước 1: Cho một lượng nhỏ bông vào cốc chứa 10 mL dung dịch H2SO4 và dùng đũa khuấy đều.

Bước 2: Đặt cốc thủy tinh vào cốc nước nóng và khuấy đến khi tạo thành dung dịch đồng nhất.

Bước 3: Thêm NaHCO3 đến khi dừng bọt khí. Sau đó thêm tiếp 5 mL dung dịch NaOH 10%.

Bước 4: Cho 5 mL dịch thu được vào ống nghiệm chứa 2 mL NaOH và 1 mL dung dịch CuSO4 (tạo thành Cu(OH)2).

Bước 5: Đun nóng ống nghiệm.

Cellulose bị thủy phân khi đun nóng với dung dịch acid vô cơ hoặc khi có mặt enzyme cellulase (thường có trong dạ dày động vật ăn cỏ). Sản phẩm cuối cùng nhận được khi thủy phân cellulose là glucose.
\(\left(C_6H_{10}O_5\right)_n+nH_2O\overset{H^+,t^o}{\rightarrow}nC_6H_{12}O_6\)
2. Phản ứng với nitric acid
Thí nghiệm 8: Phản ứng của cellulose với nitric acid
Bước 1: Cho khoảng 5 mL dung dịch HNO3 đặc vào ống cốc thủy tinh ngâm trong chậu nước đá. Thêm 10 mL dung dịch H2SO4 đặc vào cốc và khuấy đều.

Bước 2: Lấy cốc thủy tinh ra và cho một nhúm bông vào dung dịch.

Bước 3: Ngâm cốc trong cốc nước nóng trong khoảng 10 phút.

Bước 4: Lấy sản phẩm ra khỏi cốc, rửa sach với nước lạnh và NaHCO3 loãng. Ép khô sản phẩm bằng giấy lọc.

Các nhóm hydroxy trong các đơn vị glucose của phân tử cellulose phản ứng với dung dịch nitric acid đặc khi có mặt dung dịch sulfuric acid đặc, tạo ra các sản phẩm như cellulose trinitrate, cellulose dinitrate tùy thuộc vào điều kiện phản ứng.
\(\left[C_6H_7O_2\left(OH\right)_3\right]_n+3nHNO_3\overset{H_2SO_4đặc}{\rightarrow}\left[C_6H_7O_2\left(ONO_2\right)_3\right]_n+3nH_2O\)
\(\left[C_6H_7O_2\left(OH\right)_3\right]_n+2nHNO_3\overset{H_2SO_4đặc}{\rightarrow}\left[C_6H_7O_2\left(OH\right)\left(ONO_2\right)_2\right]_n+2nH_2O\)
3. Tác dụng với nước Schweizer
Thí nghiệm 9: Tác dụng của cellulose với nước Schweizer
Bước 1: Thêm khoảng 20 mL dung dịch NaOH 20% vào cốc chứa 50 mL dung dịch CuSO4, khuấy đều.

Bước 2: Lọc tách kết tủa và thêm khoảng 50 mL dung dịch NH3 đặc, khuấy đều đến khi kết tủa tan hết.
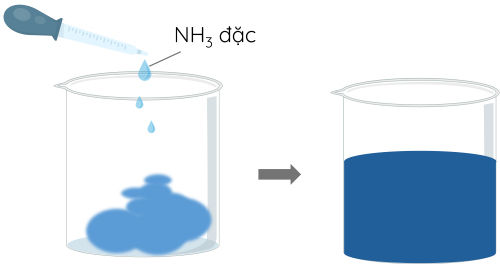
Bước 3: Thêm một lượng nhỏ bông vào nước Schweizer và khuấy đều.
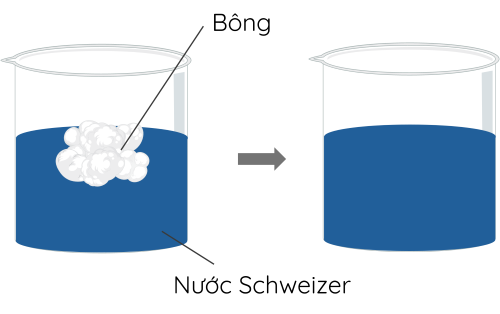
Cellulose không tan trong nước nhưng tan trong nước Schweizer (dung dịch chứa phức chất của ion Cu2+ với ammonia).
1. Glucose, fructose và saccharose thể hiện tính chất hóa học của polyalcohol; glucose và fructose còn thể hiện tính chất của nhóm carbonyl. Nhóm -OH hemiacetal bị thay thể bằng nhóm -OR khi cho glucose tác dụng với alcohol ROH. Thủy phân disaccharide (maltose, saccharose), polysaccharide (tinh bột, cellulose) sẽ tạo thành các monosaccharide.
2. Tinh bột tạo với iodine hợp chất màu xanh tím. Phản ứng màu này được sử dụng để nhận biết tinh bột bằng iodine hoặc ngược lại.
3. Cellulose tan trong nước Schweizer và tác dụng với dung dịch nitric acid khi có mặt dung dịch sulfuric acid đặc, tạo cellulose trinitrate hoặc cellulose dinitrate.

Bạn có thể đánh giá bài học này ở đây