Câu 1: Tính phần trăm khối lượng của các nguyên tố trong hợp chất: NaNO3; K2CO3 , Al(OH)3, SO2, SO3, Fe2O3.
Câu 2: Xác định CTHH của hợp chất giữa nguyên tố X với O có %X = 43,67%. Biết X có hóa trị V trong hợp chất với O. (ĐS: P2O5)
Câu 3: Hợp chất B có %Al = 15,79%; %S = 28,07%, còn lại là O. Biết khối lượng mol B là 342.Viết CTHH dưới dạng Alx(SO4)y .Xác định CTHH. (ĐS: Al2(SO4)3 )
Câu 4: Một hợp chất khí X có tỉ khối đối với hidro là 8,5. Hãy xác định công thức hóa học của X biết hợp chất khí có thành phần theo khối lượng là 82,35% N và 17,65% H.(ĐS: NH3)
Câu 5: Một hợp chất X của S và O có tỉ khối đối với không khí là 2,207.
a. Tính MX (ĐS: 64 đvC)
b. Tìm công thức hóa học của hợp chất X biết nguyên tố S chiếm 50% khối lượng, còn lại là O. (ĐS: SO2)
Dạng bài tập 6: Tính theo phương trình hóa

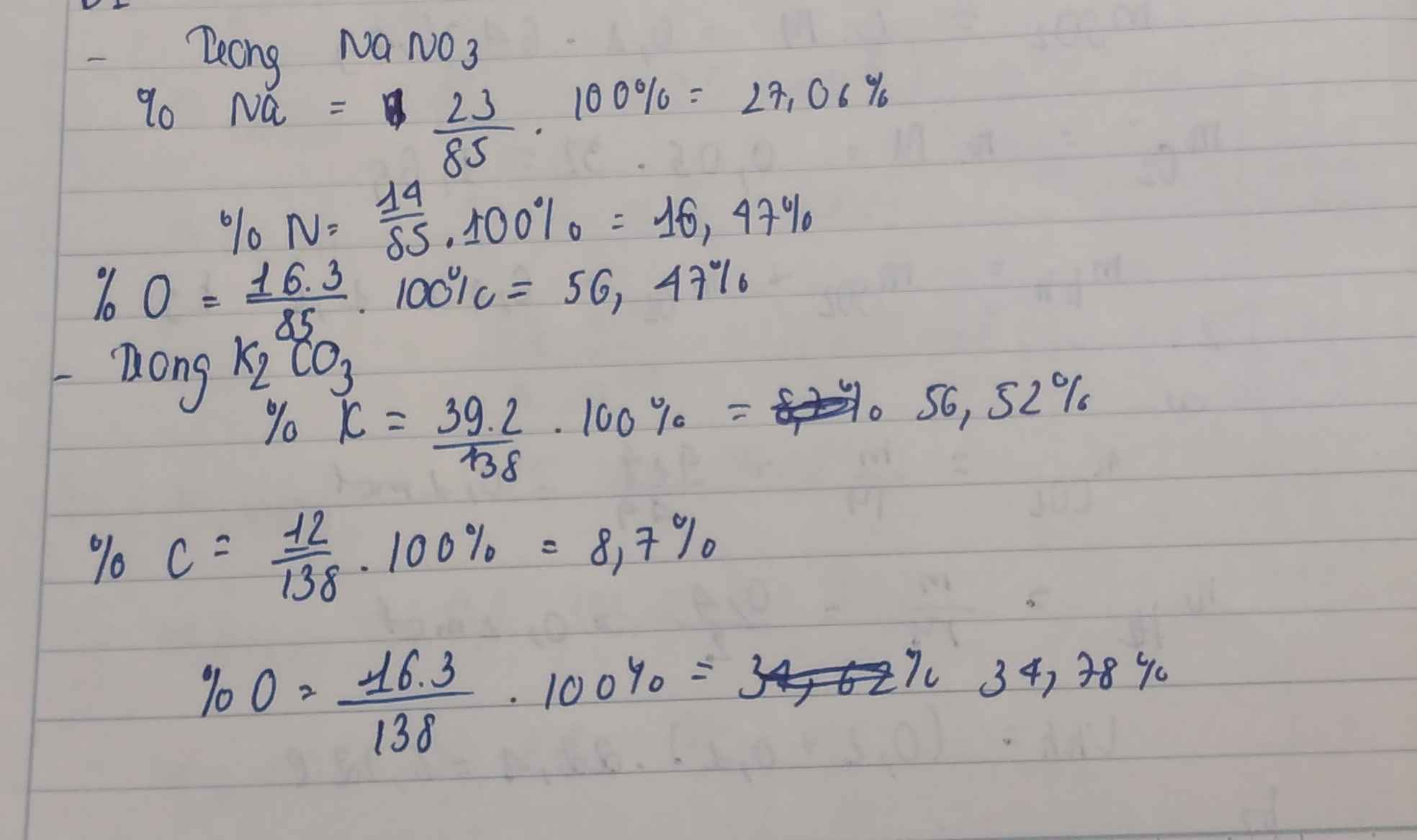
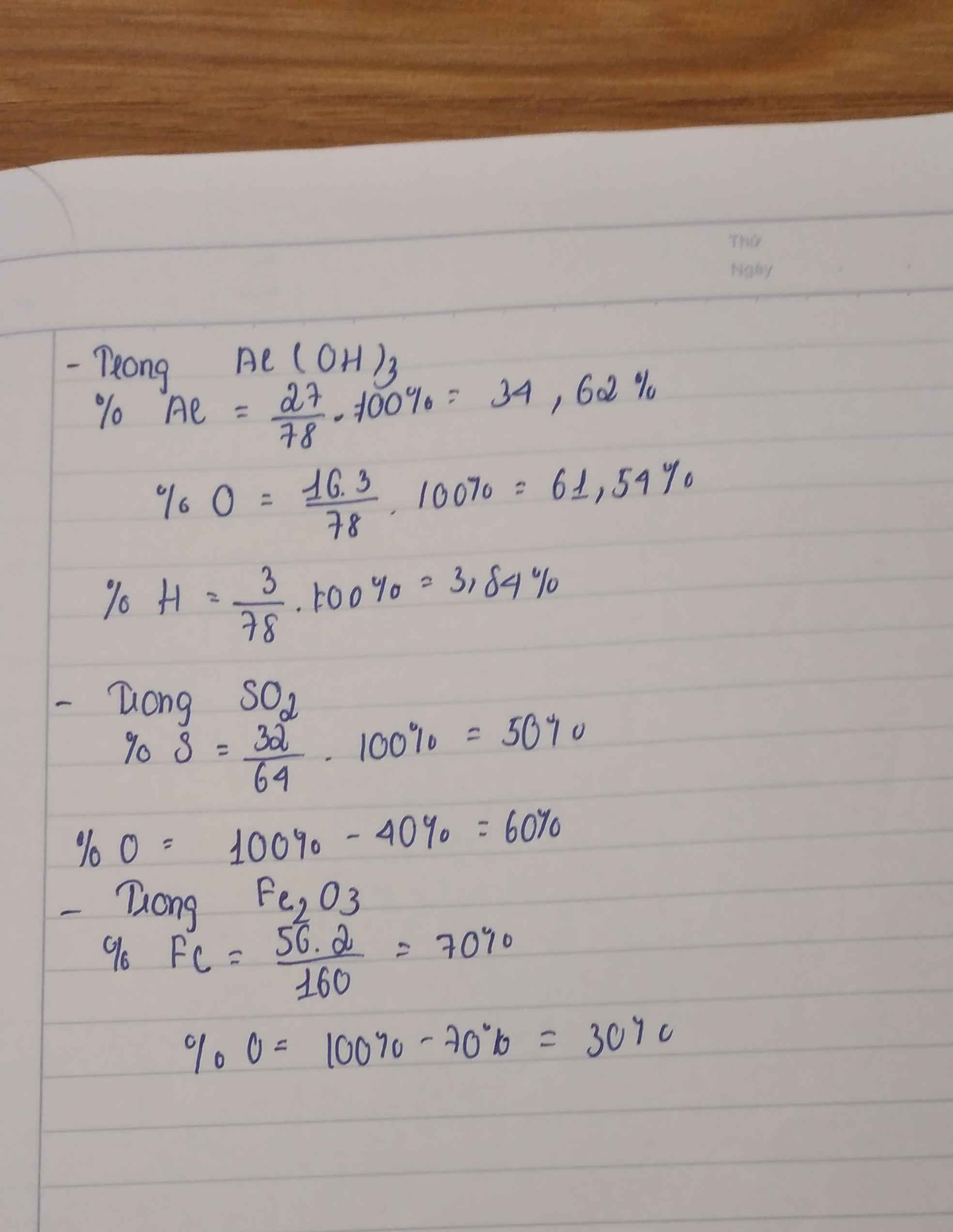
Câu 2:
\(CTHH:X_2O_5\\ M_{X_2O_5}=\dfrac{16}{100\%-43,67\%}=142\left(g\text{/}mol\right)\\ \Rightarrow M_X=\dfrac{142-16.5}{2}=31\left(g\text{/}mol\right)\left(P\right)\\ \Rightarrow CTHH:P_2O_5\)
Câu 3:
Trong 1 mol B: \(\left\{{}\begin{matrix}n_{Al}=\dfrac{342.15,79\%}{27}=2\left(mol\right)\\n_S=\dfrac{342.28,07\%}{32}=3\left(mol\right)\\n_O=\dfrac{342-2.27-3.32}{16}=12\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow CTHH_B:Al_2\left(SO_4\right)_3\)
Câu 4:
\(M_X=8,5.2=17\left(g\text{/}mol\right)\)
Trong 1 mol X: \(\left\{{}\begin{matrix}n_N=\dfrac{17.82,35\%}{14}=1\left(mol\right)\\n_H=\dfrac{17.17,65\%}{1}=3\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow CTHH_X:NH_3\)
C1:
\(NaNO3:\)
\(MNaNO3=23+62=\dfrac{85g}{mol}\)
\(\%Na=\dfrac{23.100}{85}=27\%\)
\(\%N=\dfrac{14.100}{85}=16\%\)
\(\%O=\dfrac{16.3.100}{85}=56\%\)
\(K2CO3\)
\(MK2CO3=39.2+60=\dfrac{138g}{mol}\)
\(\%K=\dfrac{39.2.100}{138}=57\%\)
\(\%C=\dfrac{12.100}{138}=9\%\)
\(\%O=\dfrac{16.3.100}{138}=35\%\)
\(Al\left(OH\right)3:\)
\(MAl\left(OH\right)3=27+17.3=\dfrac{78g}{mol}\)
\(\%Al=\dfrac{27.100}{78}=35\%\)
\(\%O=\dfrac{16.3.100}{78}=62\%\)
\(\%H=\dfrac{1.3.100}{78}=4\%\)
\(SO2:\)
\(MSO2=32+16.2=\dfrac{64g}{mol}\)
\(\%S=\dfrac{32.100}{64}=50\%\)
\(\%O=\dfrac{16.2.100}{64}=50\%\)
\(SO3:\)
\(MSO3=32+16.3=\dfrac{80g}{mol}\)
\(\%S=\dfrac{32.100}{80}=40\%\)
\(\%O=\dfrac{16.3.100}{80}=60\%\)
\(Fe2O3:\)
\(MFe2O3=56.2+16.3=\dfrac{160g}{mol}\)
\(\%Fe=\dfrac{56.2.100}{160}=70\%\)
\(\%O=\dfrac{16.3.100}{160}=30\%\)
C5:
a,MX=2,207.29=64đvC
b, gọi cthh của hợp chất này là SxOy
Ta có: 32x:16y=50:50
=>x:y=\(\dfrac{50}{32}:\dfrac{50}{16}\)
= 1,5625:3,125
= 1 : 2
Vậy CTHH của hợp chất này là SO2
C2,3,4 lm r nên t bổ sung thim:>