đốt cháy hoàn toàn 20,8(g) hỗn hợp gồm Ca và Cu trong bình chứa 4,48(l) O2 vừa đủ( đktc)
a) tính thành phần phần trăm mỗi kim loại ban đầu
b) tính khối lượng mỗi oxit thu được
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

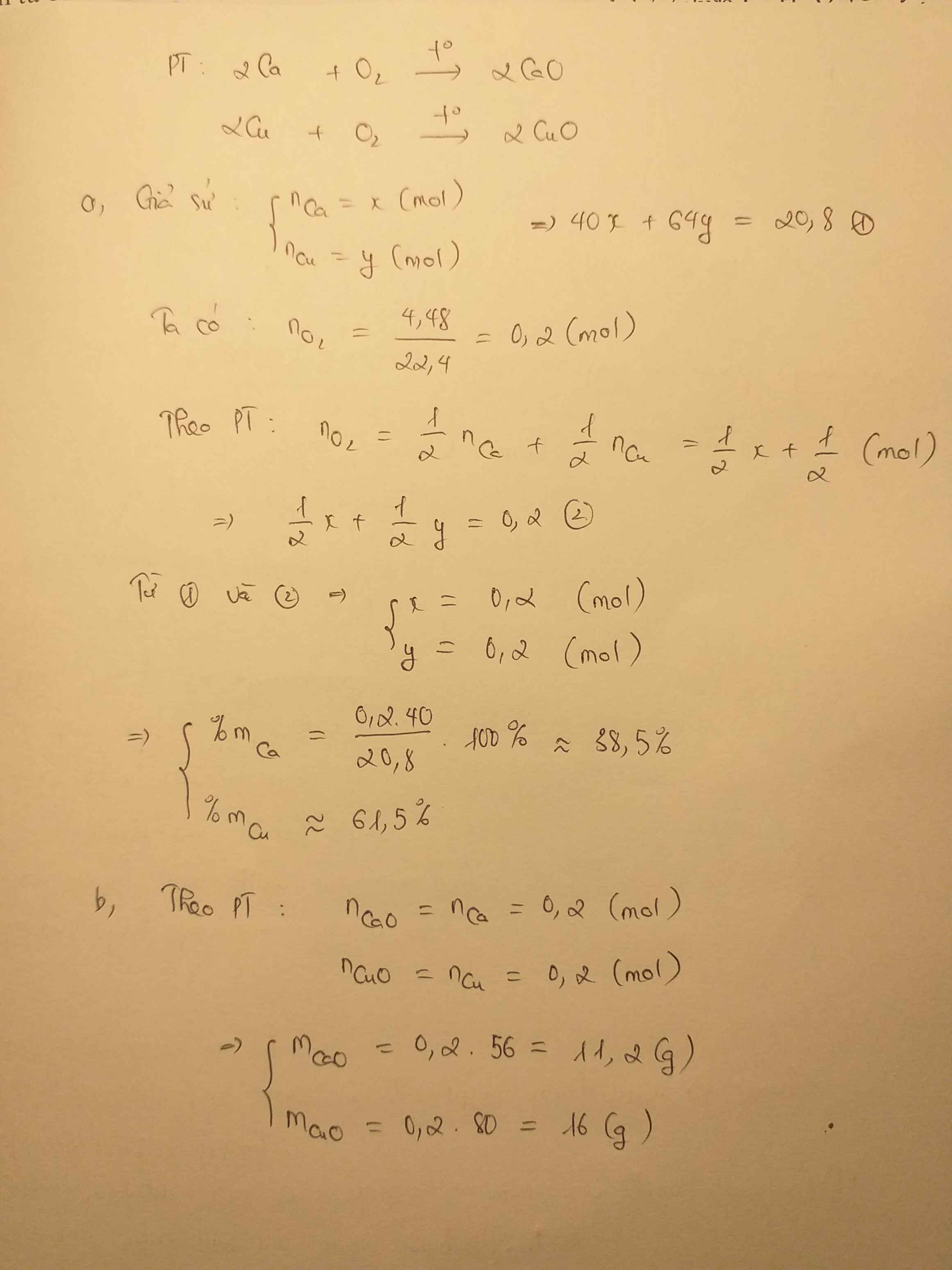

a)
Dung dịch X gồm $Ca(OH)_2,Ba(OH)_2$ làm đổi màu quỳ tím chuyển màu xanh.
b)
$Ca + 2H_2O \to Ca(OH)_2 + H_2$
$Ba + 2H_2O \to Ba(OH)_2 + H_2$
Gọi $n_{Ca} = a ; n_{Ba} = b$
Ta có :
$m_{hh} = 40a + 137b = 17,7(gam)$
$n_{H_2} = a + b = 0,2(mol)$
Suy ra a = b = 0,1
$\%m_{Ca} = \dfrac{0,1.40}{17,7}.100\% = 22,6\%$
$\%m_{Ba} = 100\%-22,6\% = 77,4\%$
c)
$n_{Ca(OH)_2} = n_{Ba(OH)_2} = a = b = 0,1(mol)$
$m_{Ca(OH)_2} = 0,1.74 = 7,4(gam)$
$m_{Ba(OH)_2} = 0,1.171 = 17,1(gam)$

nH2 = 13,44/22,4 = 0,6 (mol)
PTHH: Mg + 2HCl -> MgCl2 + H2
nHCl = 0,6 . 2 = 1,2 (mol)
mHCl = 1,2 . 36,5 = 43,8 (g)
nMg = 0,6 (mol)
mMg = 0,6 . 24 = 14,4 (g)
Không thấy mhh để tính%

a, Giả sử: \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
⇒ 27x + 56y = 13,8 (1)
BTNT Al và Fe, có: \(\left\{{}\begin{matrix}n_{Al_2O_3}=\dfrac{1}{2}n_{Al}=\dfrac{1}{2}x\left(mol\right)\\n_{Fe_3O_4}=\dfrac{1}{3}n_{Fe}=\dfrac{1}{3}y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\dfrac{1}{2}x.102+\dfrac{1}{3}y.232=21,8\left(g\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2.27}{13,8}.100\%\approx39,1\%\\\%m_{Fe}\approx60,9\%\end{matrix}\right.\)
b, BTNT O, có: \(n_{O_2}=\dfrac{3n_{Al_2O_3}+4n_{Fe_3O_4}}{2}=0,6\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,6.22,4=13,44\left(l\right)\)
Bạn tham khảo nhé!

PTHH: \(2Mg+O_2\underrightarrow{t^o}2MgO\) (1)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\) (2)
a) Gọi số mol của Mg là a (mol) \(\Rightarrow n_{Al}=\dfrac{2}{3}a\left(mol\right)\)
\(\Rightarrow24a+27\cdot\dfrac{2}{3}a=6,3\) \(\Rightarrow a=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{MgO}=0,15\left(mol\right)\\n_{Al_2O_3}=0,05\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{MgO}=0,15\cdot40=6\left(g\right)\\m_{Al_2O_3}=0,05\cdot102=5,1\left(g\right)\end{matrix}\right.\)
b) Theo các PTHH: \(\left\{{}\begin{matrix}n_{O_2\left(1\right)}=0,075\left(mol\right)\\n_{O_2\left(2\right)}=0,075\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\Sigma n_{O_2}=0,15\left(mol\right)\) \(\Rightarrow V_{O_2}=0,15\cdot22,4=3,36\left(l\right)\)

má ơi tốc độ thân thánh thế em? Em tự làm nhanh hơn anh gõ máy

\(a)\\ 4Al+ 3O_2 \xrightarrow{t^o} 2Al_2O_3\\ 3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4\\ \)
b) Bảo toàn khối lượng :
\(m_{O_2} = 21,8 -13,8 =8(gam)\\ n_{O_2} = \dfrac{8}{32} = 0,25(mol)\\ V_{O_2} = 0,25.22,4 = 5,6(lít)\)
c)
\(n_{Al} = a(mol) ; n_{Fe} = b(mol)\Rightarrow 27a + 56b = 13,8(1)\\ n_{O_2} = 0,75a + \dfrac{2}{3}b = 0,25(2)\\ (1)(2)\Rightarrow a = 0,2 ; b = 0,15\\ \%m_{Al} = \dfrac{0,2.27}{13,8}.100\% =39,13\%\\ \%m_{Fe} = 100\% -39,13\% = 60,87\%\)

\(a) n_{Mg}= a(mol) ; n_{Al} = b(mol) \Rightarrow 24a + 27b =2,55(1)\\ Mg + 2HCl \to MgCl_2 + H_2\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ n_{H_2} = a + 1,5b = \dfrac{2,8}{22,4}=0,125(2)\\ (1)(2) \Rightarrow a = b = 0,05\\ \%m_{Mg} = \dfrac{0,05.24}{2,55}.100\% = 47,06\%\ ;\ \%m_{Al} =100\% -47,06\% = 52,94\%\\ b) n_{HCl} = 2n_{H_2} = 0,125.2 = 0,25(mol)\\ m_{dd\ HCl} = \dfrac{0,25.36,5}{7,3\%} = 125(gam)\\ V_{dd\ HCl} = \dfrac{125}{1,2} = 104,17(ml)\)