Hoà tan hoàn toàn 7,8 gam hỗn hợp Al và Mg trong dung dịch H2SO4 đăc nóng thu được 8,96 lit khí SO2 ( đtkc) . Xác định thành phần phần trăm về khối lượng của mỗi kim loại trong hỗn hợp.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{SO_2}=\dfrac{8,4}{22,4}=0,375\left(mol\right)\)
PTHH: \(2Al+6H_2SO_4\underrightarrow{t^o}Al_2\left(SO_4\right)_3+3SO_2+6H_2O\\ Mg+2H_2SO_4\underrightarrow{t^o}MgSO_4+SO_2+2H_2O\)
Đặt \(n_{Al}=a\left(mol\right);n_{Mg}=b\left(mol\right)\)
Ta có \(\left\{{}\begin{matrix}27a+24b=7,65\\1,5a+b=0,375\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}a=0,15\\b=0,15\end{matrix}\right.\)
\(\%m_{Al}=\dfrac{27.0,15}{7,65}.100\%=52,94\%\\ \%m_{Mg}=100\%-52,94\%=47,06\%\)

\(n_{H_2}=\dfrac{8,96}{22,4}=0,4(mol)\\ n_{Al}=x(mol);n_{Mg}=y(mol)\\ \Rightarrow 27x+24y=7,8(1)\\ a,2Al+6HCl\to 2AlCl_3+3H_2\\ Mg+2HCl\to MgCl_2+H_2\\ \Rightarrow 1,5x+y=0,4(2)\\ (1)(2)\Rightarrow x=0,2(mol);y=0,1(mol)\\ \Rightarrow \%_{Al}=\dfrac{0,2.27}{7,8}.100\%=69,23\%\\ \Rightarrow \%_{Mg}=100\%-69,23\%=30,77\%\)
\(b,\Sigma n_{HCl}=3x+2y=0,8(mol)\\ \Rightarrow C\%_{HCl}=\dfrac{0,8.36,5}{192,2}.100\%=15,19\%\\ c,n_{AlCl_3}=0,2(mol);n_{MgCl_2}=0,1(mol)\\ \Rightarrow C\%_{AlCl_3}=\dfrac{0,2.133,5}{0,2.27+192,2-0,3.2}.100\%=13,55\%\\ C\%_{MgCl_2}=\dfrac{0,1.95}{0,1.24+192,2-0,1.2}.100\%=4,89\%\)

\(n_{Fe}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(m_{hh}=56a+27b=11\left(g\right)\left(1\right)\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(n_{H_2}=a+1.5b=0.4\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.2\)
\(\%Fe=\dfrac{0.1\cdot56}{11}\cdot100\%=50.91\%\)
\(\%Al=49.09\%\)

Quy đổi hỗn hợp X thành Fe (a mol) và O (b mol)
Các quá trình nhường và nhận electron:
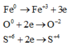
Theo định luật bảo toàn khối lượng ta có: 56a + 16b = 49,6 (1)
Theo định luật bảo toàn electron ta có: 0,4.2 + 2b = 3a (2)
(1) và (2) => a = 0,7; b = 0,65 (mol)
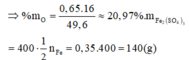
Đáp án A

Không viết phương trình nhá !!
a) Gọi a và b lần lượt là số mol của Mg và Al
\(\Rightarrow24a+27b=1,035\) (1)
Ta có: \(n_{H_2}=\dfrac{1,176}{22,4}=0,0525\left(mol\right)\)
Bảo toàn electron: \(2a+3b=2\cdot0,0525\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,015\\b=0,025\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,015\cdot24}{1,035}\cdot100\%\approx34,78\%\\\%m_{Al}=65,22\%\end{matrix}\right.\)
b) Ta có: \(\left\{{}\begin{matrix}\Sigma n_{H_2SO_4}=\dfrac{100\cdot9,8\%}{98}=0,1\left(mol\right)\\n_{H_2SO_4\left(p/ứ\right)}=n_{H_2}=0,0525\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{H_2SO_4\left(dư\right)}=0,0475\left(mol\right)\) \(\Rightarrow m_{H_2SO_4\left(dư\right)}=0,0475\cdot98=4,655\left(g\right)\)
c) Bảo toàn nguyên tố: \(\left\{{}\begin{matrix}n_{Al_2O_3}=\dfrac{1}{2}n_{Al}=0,0125\left(mol\right)\\n_{MgO}=n_{Mg}=0,015\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{oxit}=0,0125\cdot102+0,015\cdot40=1,875\left(g\right)\)
a) Gọi \(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\end{matrix}\right.\)
\(m_A=1,035\left(g\right)\rightarrow24a+27b=1,035\) (1)
\(Mg+2H_2SO_4đ\rightarrow MgSO_4+SO_2+2H_2O\)
a ------------ 2a ----------------------- a (mol)
\(2Al+6H_2SO_4đ\rightarrow Al_2\left(SO_4\right)_3+3SO_2+6H_2O\)
b ------------ 3b -------------------------- 1,5b (mol)
\(n_{SO_2}=\dfrac{1,176}{22,4}=0,0525\left(mol\right)\rightarrow a+1,5b=0,0525\) (2)
Giải hệ (1)(2) \(\rightarrow\left\{{}\begin{matrix}a=0,015\\b=0,025\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{Mg}=0,015.24=0,36\left(g\right)\\m_{Al}=0,025.27=0,675\left(g\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}\%m_{Mg}=34,78\%\\\%m_{Al}=65,22\%\end{matrix}\right.\)
b) \(\Sigma_{n_{H_2SO_4}}=2a+3b=0,105\left(mol\right)\)
\(\rightarrow m_{H_2SO_4}=0,105.98=10,29\left(g\right)\)
c. \(\left\{{}\begin{matrix}n_{MgO}=n_{Mg}=0,015\left(mol\right)\\n_{Al_2O_3}=\dfrac{1}{2}.n_{Al}=0,0125\left(mol\right)\end{matrix}\right.\)
\(\rightarrow m_{oxit}=0,015.40+0,0125.102=1,875\left(g\right)\)

Gọi x,y lần lượt là số mol của Al, Fe
nH2 = \(\dfrac{8,96}{22,4}\)=0,4 mol
Pt: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
......x.................................0,5x...........1,5x
.....Fe + H2SO4 --> FeSO4 + H2
.......y..........................y............y
Ta có hệ pt:
{27x+56y=11
1,5x+y=0,4
⇔x=0,2, y=0,1
% mAl = \(\dfrac{0,2.27}{11}\).100%=49,1%
% mFe = \(\dfrac{0,1.56}{11}\).100%=50,9%
mAl2(SO4)3 = 0,5x . 342 = 0,5 . 0,2 . 342 = 34,2 (g)
mFeSO4 = 152y = 152 . 0,1 = 15,2 (g)
Gọi CTTQ: MxOy
Pt: MxOy + yH2 --to--> xM + yH2O
\(\dfrac{0,4}{y}\)<-------0,4
Ta có: 232,2=\(\dfrac{0,4}{y}\)(56x+16y)
⇔23,2=\(\dfrac{22,4x}{y}\)+6,4
⇔\(\dfrac{22,4x}{y}\)=16,8
⇔22,4x=16,8y
⇔x:y=3:4
Vậy CTHH của oxit: Fe3O4
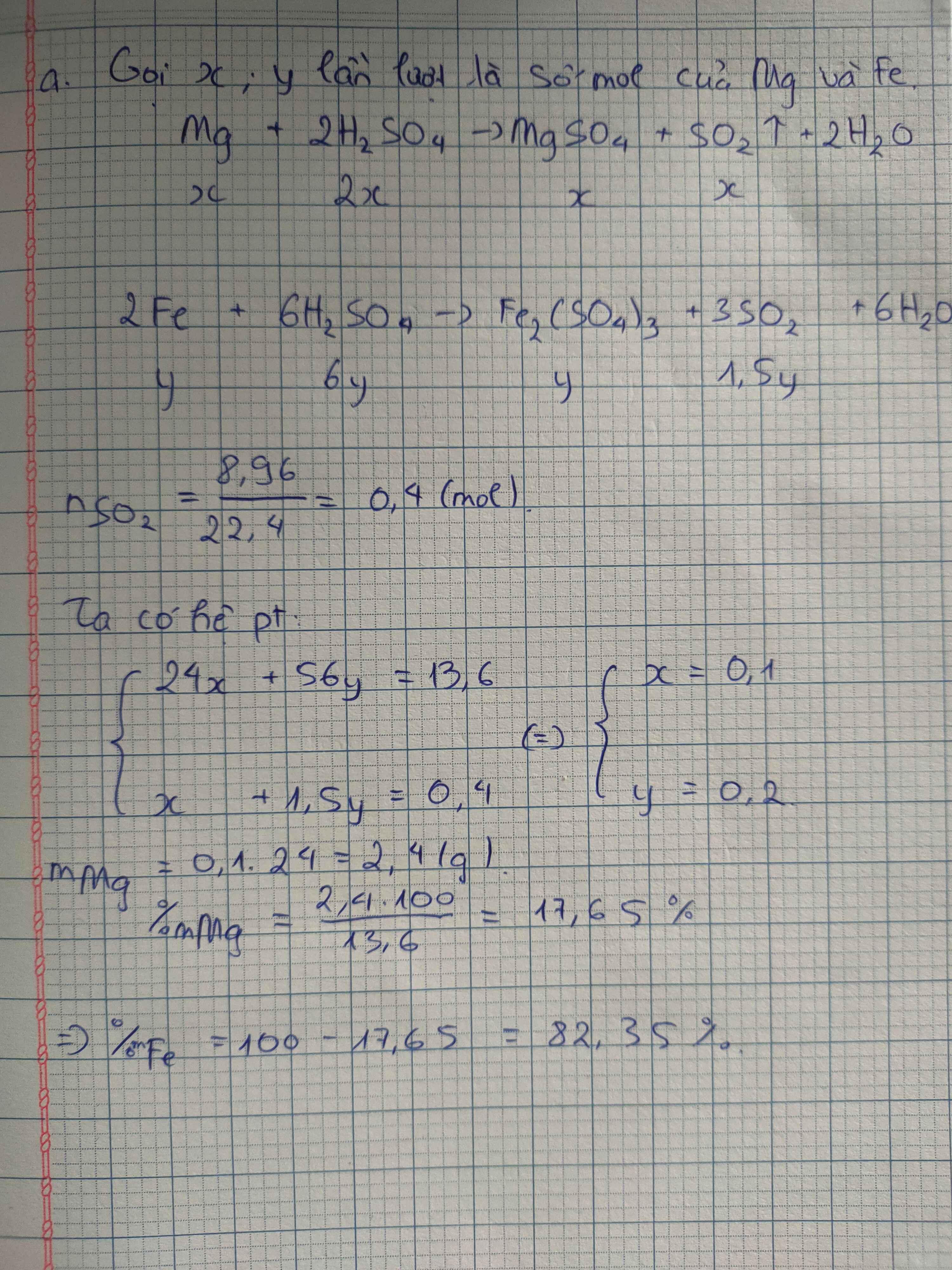


nSO2= 0,4(mol)
Đặt: nAl=a(mol); nMg=b(mol) (a,b>0)
PTHH: 2 Al + 6 H2SO4(đ) -to-> Al2(SO4)3 + 3 SO2 + 6 H2O
a____________3a______0,5a___________1,5a(mol)
Mg + 2 H2SO4(đ) -to-> MgSO4 + SO2 + 2 H2O
b_____2b________b________b(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}27a+24b=7,8\\1,5a+b=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
=> mMg=0,1.24=2,4(g)
=>%mMg=(2,4/7,8).100=30,769%
=> %mAl= 69,231%