Các thầy cô cho em hỏi tí,ở lớp với bài tập hóa em toàn gặp phải bài nói là chất này tác dụng với O2 dư hay HCl dư;AgNO3 dư, em chả hiểu từ ''dư'' là gì, mong thầy cô giải thích cho em hiểu ạ. Em cảm ơn.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{H_2}=\dfrac{13.44}{22.4}=0.6\left(mol\right)\)
\(n_{M\left(pu\right)}=a\left(mol\right)\)
Bảo toàn e :
\(na=0.15\cdot4+0.6\cdot2=1.8\)
\(a=\dfrac{1.8}{n}\)
\(M=\dfrac{16.2}{\dfrac{1.8}{n}}=9n\)
\(n=3\Rightarrow M=27.M:Al\)

Có: nKMnO4=6,951/158= 0,044 mol
2KMnO4+ 16HCl= 2KCl+ 2MnCl2+ 5Cl2+ 8H2O (1)
nCl2= 2,5nKMno4= 2,5.0,044=0,11 mol
Gọi KL cần tìm là M có hóa trị x khi phản ứng với Cl2 và có hóa trị là y khi phản ứng với HCl
2M+ xCl2=(t0) 2MClx (2)
P1: 2M+2y HCl= 2MCly +y H2 (3)
Do phản ứng (3) có khí thoát ra nên phản ứng (2) có kim loại dư.
Ta có: nH2= 0,112/22,4= 0,005 mol
nM(3)= 0,005.2/y=0,01/y mol ---> nMdư sau pư (2)= 0,02/y mol( do chia thành chất rắn tạo thành thành 2 phần bằng nhau)
nM(2)= 0,11.2/x=0,22/x mol
=> mM= (0,02/y+0,22/x).MM=7,8 suy ra MM=7,8xy/(0,02x+0,22y)
x=y=1 ==> MM=32,5( loại)
x=3; y=2 ==> MM=93,6( loại)
x=y=3 ==> MM= 97,5( loại)
x=y=2 ==> MM=65 (Zn)
P2: Zn+ Cu(NO3)2= Zn(NO3)2+ Cu (4)
nZn(4)= nZn(3)= 0,01/y=0.01/2= 0,005 mol --> mCu= 0,005.64=0,32 g

\(n_M=\dfrac{16,2}{M_M}\left(mol\right)\); \(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: 4M + aO2 --to--> 2M2Oa
____\(\dfrac{0,6}{a}\)<--0,15
2M + 2aHCl --> 2MCla + aH2
\(\dfrac{1,2}{a}\)<-------------------------0,6
=> \(\dfrac{0,6}{a}+\dfrac{1,2}{a}=\dfrac{16,2}{M_M}=>M_M=9a\left(g/mol\right)\)
Xét a = 1 => MM = 9 (L)
Xét a = 2 => MM = 18 (L)
Xét a = 3 => MM = 27 (Al)

Bài 1:
a) nP=6,2/31=0,2(mol); nO2= 6,72/22,4=0,3(mol)
PTHH: 4P + 5 O2 -to-> 2 P2O5
Ta có: 0,2/4 < 0,3/5
=> P hết, O2 dư, tính theo nP
=> nO2(p.ứ)= 5/4. nP= 5/4. 0,2=0,25(mol)
=> mO2(dư)=0,3- 0,25=0,05(mol)
=> mO2(dư)=0,05.32=1,6(g)
b) nP2O5= nP/2= 0,2/2=0,1(mol)
=>mP2O5=0,1.142=14,2(g)

n KClO3 = 4,9/122,5 = 0,04(mol)
$2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2$
n O2 = 3/2 n KClO3 = 0,06(mol)
X cho vào HCl thấy thoát ra khí chứng tỏ X chứa R dư
Gọi n là hóa trị của R
n H2 = 1,344/22,4 = 0,06(mol)
$4R + nO_2 \xrightarrow{t^o} 2R_2O_n$
$2R + 2nHCl \to 2RCl_n + nH_2$
n R = 4/n n O2 + 2/n n H2 = 0,36/n(mol)
Bảo toàn khối lượng :
=> m R = m X - m O2 = 6,24 - 0,06.32 = 4,32(gam)
Suy ra :
0,36/n . R = 4,32
=> R = 12n
Với n = 2 thì R = 24(Magie)

Đáp án D
Đặt Zn, Cr,Sn là x mol → ZnCl2 : x mol, SnCl2 : x mol và CrCl2 : x mol
→ x =0,02 mol
Bảo toàn O trong phương trình đốt cháy có 2nO2 = x + 2x + 3/2 x =0,09
→ VO2= 1,008 lít
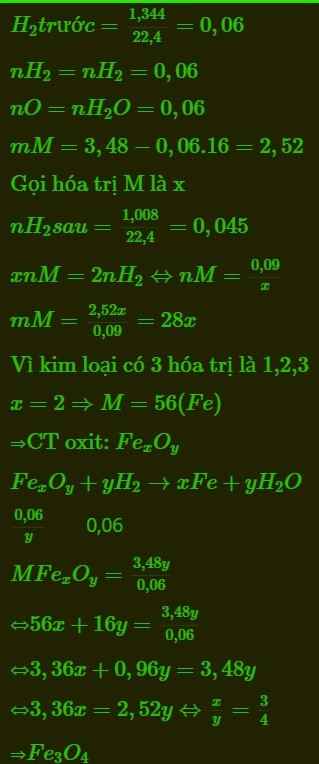

ví dụ fe tác dụng với hcl dư tạo thành fecl2 và h2
=> nfecl2 và nh2 sẽ được tính theo fe vì lượng fe pư hết, hcl dư đó bạn
và lượng hcl pư hết cũng đc tính theo lượng fe: nhcl pư= 2nfe
nhcl dư=nhcl ban đầu- nhcl pư hếT
TÓM LẠI TRONG BÀI TOÁN ĐỀ CHO 1 CHẤT DƯ THÌ CHẤT CÒN LẠI SẼ PƯ HẾT, VÀ CÁC CHẤT THU ĐƯỢC TÍNH THEO CHẤT PƯ HẾT ĐÓ BẠN!
mong bạn sẽ hiêu
tứ là những chất tham gia sau khi phản ứng vẫn chưa phản ứng hết thì gọi là dư