Có 3 bình mất nhãn, mỗi bình chứa một hỗn hợp dung dịch sau: Na2SO4 và K2CO3; KHCO3 và Na2CO3; KHCO3 và Na2SO4. Trình bày phương pháp hóa học để nhận biết 3 bình này mà chỉ cần dùng thêm dung dịch HCl và Ba(NO3)2 làm thuốc thử. Viết các phương trình hóa học xảy ra.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Nhỏ từ từ $HCl$ vào 3 mẫu thử. Lọ nào không xuất hiện khí ngay chứa $Na_2CO_3$ và $K_2SO_4$. Hai lọ còn lại tạo khí ngay lập tức
Nhỏ $BaCl_2$ vào hai lọ còn lại tới khi thấy kết tủa không tăng thì đem nhỏ $HCl$ tới dư. Lọ nào vẫn cho kết tủa thì chứa $KHCO_3$ và $Na_2SO_4$
Lọ còn lại chứa $K_2CO_3$ và $NaHCO_3$
Trích mẫu thử
Cho từ từ dd HCl vào mẫu thử
- MT xuất hiện khí ngay là $KHCO_3$ và $Na_2SO_4$
- MT sau một thời gian mới xuất hiện khí là $K_2CO_3$ và $NaHCO_3$ ; $Na_2CO_3$ và $K_2SO_4$
Cho dung dịch $BaCl_2$ tới dư vào hai mẫu thử còn. Sau đó thêm lượng dư dung dịch $HCl$
- MT nào tạo kết tủa rồi tan hết là $K_2CO_3,NaHCO_3$
- MT nào không tan hoàn toàn là $Na_2CO_3,K_2SO_4$
$K_2CO_3 + HCl \to KCl + KHCO_3$
$NaHCO_3 + HCl \to NaCl + CO_2 + H_2O$
$KHCO_3 + HCl \to KCl + CO_2 + H_2O$
$Na_2CO_3 + HCl \to NaCl + NaHCO_3$
$BaCl_2 +K_2CO_3 \to BaCO_3 + 2KCl$
$BaCl_2 + K_2SO_4 \to BaSO_4 + 2KCl$
$BaCO_3 + 2HCl \to BaCl_2 + CO_2 + H_2O$

Đáp án B
Để phân biệt các dung dịch NaNO3, H2SO4, Na2SO4, NaOH người ta dùng : quì tím, dung dịch BaCl2 vì
|
|
NaNO3 |
H2SO4 |
Na2SO4 |
NaOH |
| Quì tím |
Tím |
Đỏ |
Tím |
Xanh |
| BaCl2 |
Không hiện tượng |
x |
Kết tủa trắng |
x |
Dấu x là đã nhận biết được rồi
Phương trình hóa học:
![]()

Đáp án D
Lấy BaCl2 cho lần lượt vào 3 mẫu thử.
Các phương trình phản ứng xảy ra:
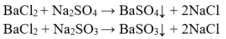
Mẫu không có kết tủa là HCl. Lấy HCl cho vào kết tủa, BaSO3 tan.
![]()

Trích mẫu thử :
Cho quỳ tím vào các mẫu thử :
+ Quỳ hóa đỏ : H2SO4
+ Quỳ hóa xanh : KOH , K2CO3 (I)
+ Quỳ không đổi màu : Na2SO4
Nhỏ dung dịch HCl vào nhóm(i) :
+ Có khí không màu thoát ra : K2CO3
Không hiện tượng : KOH
\(K_2CO_3+2HCl\rightarrow2KCl+H_2O+CO_2\)
\(KOH+HCl\rightarrow KCl+H_2O\)

\(n_{Br_2}=\dfrac{64}{160}=0,4\left(mol\right)\)
\(n_{hh}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,4<----0,4
\(\rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,4}{0,5}.100\%=80\%\\\%V_{CH_4}=100\%-80\%=20\%\end{matrix}\right.\)
\(C_{M\left(Br_2\right)}=\dfrac{0,4}{0,25}=1,6M\)

\(n_{Br_2}=\dfrac{64}{160}=0,4\left(mol\right)\\ n_{hh2khi}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\\ ChỉcóC_2H_4tácdụngvớiBr_2\\ PTHH:C_2H_4+Br_2\rightarrow C_2H_4Br_2\\ n_{C_2H_4}=n_{Br_2}=0,4\left(mol\right)\\ \Rightarrow n_{CH_4}=0,5-0,4=0,1\left(mol\right)\\ \%Vcũnglà\%n\\ \Rightarrow\%V_{CH_4}=\dfrac{0,1}{0,5}.100=20\%;\%V_{C_2H_4}=100-20=80\%\\ CM_{Br_2}=\dfrac{0,4}{0,25}=1,6M\)

\(n_{hhk}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\) ; \(n_{Br_2}=\dfrac{64}{160}=0,4\left(mol\right)\)
\(C_2H_4+Br_{2\left(dd\right)}\rightarrow C_2H_4Br_2\)
0,4 0,4 ( mol )
\(\left\{{}\begin{matrix}V_{C_2H_4}=0,4.22,4=8,96\left(l\right)\\V_{CH_4}=11,2-8,96=2,24\left(l\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,4}{0,5}.100=80\%\\\%V_{CH_4}=100-80=20\%\end{matrix}\right.\)
\(C_{M_{Br_2}}=\dfrac{0,4}{0,25}=1,6\left(M\right)\)