hỗn khí A gồm cacbon oxit và không khí .trong đó tỉ lệ thể tích của khí cacbon oxit và không khí lần lượt là 3:5 (trong không khí thì khí oxi chiếm 20% thể tích ;còn lại là nito) .đốt cháy hỗn hợp khí A một thời gian thu được hỗn hợp khí B .trong B thì phần trăm thể tích của nito tăng 3,33% so với nito trong A .tính phần trăm thể tích của mỗi khí trong B .
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi a , b là số mol của KCLO3 và KMnO4
T/h 1 : Y có CO2 , N2 , O2 dư
KCLO3 ----> KCL + 3/2 O2
2 KMnO4 -----> K2MnO4 + MnO2 + O2
Gọi nO2 = x => nO2 / kk = 3x * 0,2 = 0.6x , nN2 = 3x*0.2 = 2.4x
hh khí gồm nO2 = 1.6x ; nN2 = 2.4x
Pt
C + O2 -----> CO2
nCO2 = nC = 0.528/12 = 0.044
hh khí gồm : nCO2 = 0.044 ; nO2 = 1.6x - 0.044 ; nN2 = 2.4x
=> 0.044 + 1.6x - 0.044 + 2.4x = 0.044*100 / 22.92
<=> x = 0.048
=> mmh đầu = mY + MO2 = 0.894*100 / 8.132 + 0.048* 32 = 12.53
T/h 2 : Y có CO , CO2 ; N2
Bảo toàn C : nCO + nCO2 = nC = 0.044 => nCO = 0.044 - nCO2
Bảo toàn O : 0.5*nCO + nCO2 = nO2 = 1.6a
Thay * vào đc : 0.5*( 0.044 - nCO2 ) + nCO2 = 1.6a => nCO2 = 3.2a - 0.044
Tổng mol hh : nCO + nCO2 + nN2 = 0.044 + 2.4a
=> ( 3.2a - 0.044 ) / ( 0.044 + 2.4a ) = 22.92/100
a \(\approx\)0.02
=> m = m rắn + mO2 = 0.894 *100/8.132 + 0.02 * 32 = 11.646 ( g )

Đáp án B
Từ mKCl = 0,894g => mY = 10,994g
Đặt nO2 tạo ra = x => nkk = 3x có nO2 = 0,75x và nN2 = 2,25x (mol)
, nCO2 = nC = 0,044 mol => nO2 dư = (x + 0,75x) – 0,044 (mol)
=> nT = nCO2.100/22,92 = nO2 dư + nN2 + nCO2
=> 1,75x – 0,044 + 2,25x + 0,044 = 0,192
=> x = 0,048 mol
=> m = mY + mO2 tạo ra = 12,53g
=>B

e lạy mấy a, mấy chị vào giải dùm e bài này với ạ!!
trời đậu!!
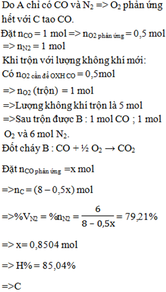
ai giúp mik vs mik cần rất gấp