Câu 21. Trong hợp chất của lưu huỳnh hàm lượng lưu huỳnh chiếm 50% . Hợp chất đó có công thức là: A. SO3B. H2SO4 C. CuS. D.SO2.Câu 22. Đốt hoàn toàn 6,72 gam than trong không khí. Thể tích CO2 thu được ở đktc là : A. 12,445 lítB. 125,44 lít C.12,544 lítD. 12,454 lít. Câu 23: Trong những oxit sau. Những oxit nào tác dụng được với dung dịch bazơ? A. CaO, CO2 Fe2O3 . ...
Đọc tiếp
Câu 21. Trong hợp chất của lưu huỳnh hàm lượng lưu huỳnh chiếm 50% . Hợp chất đó có công thức là:
A. SO3
B. H2SO4
C. CuS.
D.SO2.
Câu 22. Đốt hoàn toàn 6,72 gam than trong không khí. Thể tích CO2 thu được ở đktc là :
A. 12,445 lít
B. 125,44 lít
C.12,544 lít
D. 12,454 lít.
Câu 23: Trong những oxit sau. Những oxit nào tác dụng được với dung dịch bazơ?
A. CaO, CO2 Fe2O3 .
B. K2O, Fe2O3, CaO
C. K2O, SO3, CaO D. CO2, P2O5, SO2
Câu 24: Khí lưu huỳnh đioxit SO2 được tạo thành từ cặp chất nào sau đây?
A. K2SO4 và HCl. B.K2SO4 và NaCl. C. Na2SO4 và CuCl2 D.Na2SO3và H2SO4
Câu 25. Để nhận biết 2 lọ mất nhãn H2SO4 và Na2SO4, ta sử dụng thuốc thử nào sau đây:
A. HCl
B. Giấy quỳ tím
C. NaOH
D.BaCl2
Câu 26: Dung dịch H2SO4 có thể tác dụng được những dãy chất nào sau đây?
A. CO2, Mg, KOH. B. Mg, Na2O, Fe(OH)3 C. SO2, Na2SO4, Cu(OH)2 D. Zn, HCl, CuO.
Câu 27: Cho dung dịch BaCl2 vào dung dịch H2SO4. Sau phản ứng có hiện tượng kết tủa:
A. Màu xanh
B. Màu đỏ
C. Màu vàng
D. Màu trắng.

Câu 28: Cho phương trình phản ứng sau: 2NaOH + X 2Y + H2O.
X, Y lần lượt là:
A. H2SO4; Na2SO4 .
B. N2O5 ; NaNO3.
C. HCl ; NaCl .
D. (A) và (B) đều đúng.
Câu 29: Để loại bỏ khí CO2 có lẫn trong hỗn hợp ( O2; CO2). Người ta cho hỗn hợp đi qua dung dịch chứa:
A. HCl
B. Na2SO4
C. NaCl
D. Ca(OH)2 .
Câu 30: Nhỏ một giọt quỳ tím vào dung dịch NaOH, dung dịch có màu xanh; nhỏ từ từ dung dịch HCl cho tới dư, vào dung dịch có màu xanh trên thì.
A. Màu xanh vẫn không thay đổi. B.Màu xanh nhạt dần rồi mất hẳn.
C. Màu xanh nhạt dần rồi mất hẳn, rồi chuyển sanh màu đỏ
D.Màu xanh đậm thêm dần.
Câu 31. Có hai lọ đựng dung dịch bazơ NaOH và Ca(OH)2. Dùng các chất nào sau đây để phân biệt hai chất trên:
A. Na2CO3 B. NaCl C. MgO D. HCl .

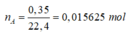
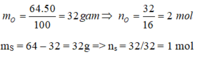
nA =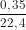 = 0,015625 mol.
= 0,015625 mol.
MA =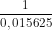 = 64g
= 64g
- Tìm số nguyên tử S, O trong phân tử A?
mO = 64 x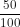 = 32g => nO =
= 32g => nO = 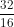 = 2 mol
= 2 mol
mS = 64 - 32 = 32g => ns =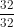 = 1 mol
= 1 mol
Suy ra trong 1 phân tử A có 1S và 2O, công thức của A là SO2
b) Khi dẫn SO2 vào dung dịch NaOH và SO2, có thể tạo thành muối trung hoà, muối axit hoặc cả hai muối:
Bài 7*. a) Hãy xác định công thức của hợp chất khí A, biết rằng :
- A là oxit của lưu huỳnh chứa 50% oxi.
- 1 gam khí A chiếm thề tích là 0,35 lít ở đktc.
b) Hoà tan 12,8 gam hợp chất khí A vào 300 ml dung dịch NaOH 1,2M. Hãy cho biết muối nào thu được sau phản ứng. Tính nồng độ mol của muối (giả thiết thể tích dung dịch thay đổi không đáng kể).
Lời giải:
nA =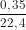 = 0,015625 mol.
= 0,015625 mol.
MA =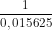 = 64g
= 64g
- Tìm số nguyên tử S, O trong phân tử A?
mO = 64 x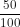 = 32g => nO =
= 32g => nO = 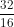 = 2 mol
= 2 mol
mS = 64 - 32 = 32g => ns =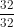 = 1 mol
= 1 mol
Suy ra trong 1 phân tử A có 1S và 2O, công thức của A là SO2
b) * Hướng dẫn: Khi dẫn SO2 vào dung dịch NaOH và SO2, có thể tạo thành muối trung hoà, muối axit hoặc cả hai muối: