Trộn 100ml dung dịch Ba(OH)2 0,5M và 100ml dung dịch KOH 0,5M thu dung dịch X. Cho X tác dụng với 100ml dung dịch H2SO4 1M. Khối lượng kết tủa và giá trị pH của dung dịch thu được sau phản ứng:
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn B
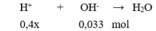
Dung dịch sau phản ứng có pH = 2 < 7 nên dung dịch sau phản ứng có H + dư
→ 0,4x – 0,033 = 10 - 2 .0,3 → x = 0,09

PTHH: \(Na_2SO_4+CaCl_2\rightarrow2NaCl+CaSO_4\downarrow\)
Ta có: \(\left\{{}\begin{matrix}n_{Na_2SO_4}=0,1\cdot0,5=0,05\left(mol\right)\\n_{CaCl_2}=0,1\cdot0,4=0,04\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Na2SO4 dư
\(\Rightarrow\left\{{}\begin{matrix}n_{CaSO_4}=0,04\left(mol\right)\\n_{NaCl}=0,08\left(mol\right)\\n_{Na_2SO_4\left(dư\right)}=0,01\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{CaSO_4}=0,04\cdot136=5,44\left(g\right)\\C_{M_{NaCl}}=\dfrac{0,08}{0,1+0,1}=0,4\left(M\right)\\C_{M_{Na_2SO_4\left(dư\right)}}=\dfrac{0,01}{0,2}=0,05\left(M\right)\end{matrix}\right.\)

Đáp án B
Gọi số mol các ion K+, HCO3-, Cl- và Ba2+ có trong 100 ml dung dịch lần lượt là x, y, z, t mol
-Phần 1: HCO3-+ OH-→ CO32-+ H2O
y y y
Ba2++ CO32-→ BaCO3
t y t mol = 0,1 mol
-Phần 2:
HCO3-+ OH-→ CO32-+ H2O
y y y
Ba2++ CO32-→ BaCO3
y y = 0,15
-Phần 3:
Ag++ Cl-→ AgCl
2z 2z = 0,2 mol suy ra z = 0,1 mol
Theo ĐLBT ĐT thì: x+2t=y+z suy ra x=0,05 mol
đun sôi đến cạn 50 ml dung dịch X thì khối lượng chất rắn khan thu được là
(39x+ 61y + 35,5.z+ 137t)/2= 14,175 gam

Fe2(SO4)3+3Ba(OH)2\(\rightarrow\)2Fe(OH)3+3BaSO4
2Fe(OH)3\(\rightarrow\)Fe2O3+3H2O
Ba(OH)2+H2SO4\(\rightarrow\)BaSO4+2H2O
Ta có
ddB+H2SO4 tạo kết tủa \(\rightarrow\)dd B là Ba(OH)2 dư
Kết tủa A gồm Fe(OH)3 và BaSO4
Chất rắn D gồm Fe2O3 và BaSO4
nBaSO4=\(\frac{0,932}{233}\)=0,004 mol
\(\rightarrow\)nBa(OH)2 dư=0,04 mol
Gọi a là số mol Fe2(SO4)3\(\rightarrow\)nBa(OH)2 tham gia=3a mol
nBaSO4=3a mol
nFe2O3=a mol
Ta có
160a+699a=4,295 \(\rightarrow\)a=0,005 mol
\(\rightarrow\) nFe2(SO4)3=0,005 mol
nBa(OH)2=0,005.3+0,004=0,019 mol
CMFe2(SO4)3=\(\frac{0,005}{0,1}\)=0,05 M
CMBa(OH)2=\(\frac{0,019}{0,1}\)=0,19 M

Đáp án D
Có n C O 2 b a n đ ầ u = 0,2; n C O 2 s ả n p h ẩ m p h ầ n 1 = 0,12; n B a C O 3 = 0,2
Dung dịch X thu được chứa K2CO3 và KOH dư hoặc K2CO3 và KHCO3
Khi cho 200 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư thu được 0,4 mol kết tủa. Dù thành phần của X gồm những chất nào thì ta luôn có:
n B a C O 3 = n C O 2 b a n đ ầ u + n K 2 C O 3
= 0,2 + y = 0,4 ⇔ y = 0,2
+) Trường hợp 1: Dung dịch X chứa K2CO3 và KOH dư.
Khi đó ở mỗi phần gọi n K 2 C O 3 = a ; n K O H = b
Bảo toàn nguyên tố C, ta có:
2a = n K 2 C O 3 b a n đ ầ u + n C O 2 b a n đ ầ u = 0,4 ⇔ a = 0,2
Khi cho 100ml dung dịch X từ từ vào 300 ml dung dịch HCl 0,5M (0,15 mol HCl) thì xảy ra các phản ứng sau:
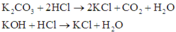
Mà thực tế nHCl < 0,24
Nên trường hợp này không thỏa mãn.
+) Trường hợp 2: Dung dịch X chứa K2CO3 và KHCO3
Khi đó ở mỗi phần gọi n K 2 C O 3 = a ; n K O H = b
Bảo toàn nguyên tố C, ta có:
n B a C O 3 = n K 2 C O 3 + n K H C O 3 = a + b = 0,2 (*)
Khi cho 100ml dung dịch X từ từ vào 300ml dung dịch HCl 0,5M (0,15 mol HCl) thì các phản ứng sau xảy ra đồng thời:
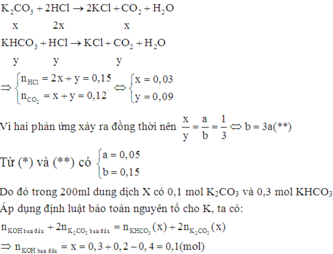

![]()
Bảo toàn C ⇒ y+0,2 = 0,2.2 = 0,4 ⇒ y = 0,2
xét 100ml X + HCl, phản ứng đồng thời
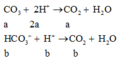
Hệ pt: a+b = 0,12 và 2a + b = 0,15
⇒ a = 0,03 và b = 0,09
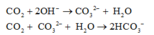
Đáp án B
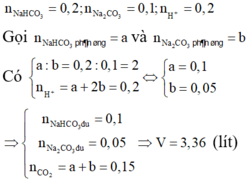

$n_{Ba^{2+}} = 0,1.0,5 = 0,05 < n_{SO_4^{2-}} = 0,1$ nên $SO_4^{2-}$ dư
$n_{BaSO_4} = n_{Ba^{2+}} = 0,05(mol)$
$m_{BaSO_4} = 0,05.233 = 11,65(gam)$
$n_{OH^-} = 0,1.0,5.2 + 0,1.0,5 = 0,15(mol)$
$n_{H^+} = 0,1.2 = 0,2(mol)$
$H^+ + OH^- \to H_2O$
$n_{H^+\ dư} = 0,2 - 0,15 = 0,05(mol)$
$V_{dd} = 0,1 + 0,1 + 0,1 = 0,3(lít)$
$[H^+] = \dfrac{0,05}{0,3} = \dfrac{1}{6}M$
$pH = -log( \dfrac{1}{6} ) = 0,778$
\(n_{Ba^{2+}}=0.1\cdot0.5=0.05\left(mol\right)\)
\(n_{OH^-}=0.1\cdot0.5\cdot2+0.1\cdot0.5=0.15\left(mol\right)\)
\(n_{H^+}=2\cdot0.1\cdot1=0.2\left(mol\right)\)
\(n_{SO_4^{2-}}=0.1\left(mol\right)\)
\(Ba^{2+}+SO_4^{2-}\rightarrow BaSO_4\)
\(0.05.........0.05.............0.05\)
\(SO_4^{2-}dư\)
\(m_{\downarrow}=0.05\cdot233=11.65\left(g\right)\)
\(H^++OH^-\rightarrow H_2O\)
\(0.15.......0.15\)
\(n_{H^+\left(dư\right)}=0.2-0.15=0.05\left(mol\right)\)
\(\left[H^+\right]=\dfrac{0.05}{0.1+0.1+0.1}=\dfrac{1}{6}\)
\(pH=-log\left(\dfrac{1}{6}\right)=0.77\)