Dẫn từ từ 1,568l khí CO2 (đktc) vào dung dịch có chứa 0,5l NaOH.Sản phẩm thu được là muối Na2CO3 và H2O. Tính nồng độ mol của dung dịch NaOH .
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(a,CO_2+Ba(OH)_2\to BaCO_3\downarrow+H_2O\\ b,n_{CO_2}=\dfrac{2,24}{22,4}=0,1(mol)\\ \Rightarrow n_{Ba(OH)_2}=0,1(mol)\\ \Rightarrow C_{M_{Ba(OH)_2}}=\dfrac{0,1}{0,2}=0,5M\\ c,n_{BaCO_3}=0,1(mol)\\ \Rightarrow m_{BaCO_3}=0,1.197=19,7(g)\)

Đáp án B
n C O 2 = 0 , 2 m o l
Cho 100 ml dung dịch X vào dung dịch chứa 0,15 mol HCl thu được 0,12 mol CO2.
Do n C O 2 < n H C l < 2 n C O 2 nên dung dịch X chứa K2CO3 và KHCO3.
Gọi số mol K2CO3 và KHCO3 phản ứng lần lượt là a, b.
=> a+b= 0,12; 2a+b=0,15
Giải được a=0,03; b=0,09 vậy trong X tỉ lệ số mol K2CO3 và KHCO3 là 1:3.
Gọi số mol K2CO3 trong X là m suy ra KHCO3 là 3m.
Cho 100 ml dung dịch X tác dụng với Ba(OH)2 dư thu được 0,2 mol kết tủa BaCO3.
Do vậy 200 ml dung dịch X tác dụng thì thu được 0,4 mol kết tủa.
=> m+3m= 0,4=> m=0,1
Bảo toàn C: n K 2 C O 3 = 0 , 4 - 0 , 2 = 0 , 2
Bảo toàn K: n K O H = 0 , 1 . 2 + 0 , 3 - 0 , 2 . 2 = 0 , 1
Vậy x= 0,1

Đáp án B
n C O 2 = 0 , 2 m o l
Cho 100 ml dung dịch X vào dung dịch chứa 0,15 mol HCl thu được 0,12 mol CO2.
Do n C O 2 < n H C l < 2 n C O 2 nên dung dịch X chứa K2CO3 và KHCO3.
Gọi số mol K2CO3 và KHCO3 phản ứng lần lượt là a, b.
=> a + b = 0,12; 2a + b = 0,15
Giải được a=0,03; b=0,09 vậy trong X tỉ lệ số mol K2CO3 và KHCO3 là 1:3.
Gọi số mol K2CO3 trong X là m suy ra KHCO3 là 3m.
Cho 100 ml dung dịch X tác dụng với Ba(OH)2 dư thu được 0,2 mol kết tủa BaCO3.
Do vậy 200 ml dung dịch X tác dụng thì thu được 0,4 mol kết tủa.
=> m + 3m = 0,4 => m = 0,1
Bảo toàn C: n K 2 C O 3 = 0,4 - 0,2 = 0,2 mol
Bảo toàn K: n K O H = 0,1.2 + 0,3 - 0,2.2 = 0,1
Vậy x=0,1
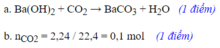

nCO2 = \(\dfrac{1,568}{22,4}=0,07\left(mol\right)\)
Pt: CO2 + 2NaOH --> Na2CO3 + H2O
0,07 mol-> 0,14 mol
CM NaOH = \(\dfrac{0,14}{0,5}=0,28M\)