Cho dd HCl 0,5M tác dụng vừa đủ với 21,6g hỗn hợp A gồm Fe,Feo,FeCO3.Thấy thoát ra một hỗn hợp khí có tỉ khối với H2 là 15 và tạo ra 31,75g muối clorua.
a.Tính thể thích dd HCl đã dùng.
b.Tính % khối lượng của mỗi chất trong A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phương trình hóa học :
Fe + 2HCl → FeCl 2 + H 2
FeO + 2HCl → FeCl 2 + H 2 O
FeCO 3 + 2HCl → FeCl 2 + H 2 O + CO 2
Tính thể tích dung dịch HCl :
n HCl = 2 n FeCl 2 = 2.31,75/127 = 0,5 mol
V HCl = 0,5/0,5 = 1l

Phương trình hóa học :
Fe + 2HCl → FeCl 2 + H 2
FeO + 2HCl → FeCl 2 + H 2 O
FeCO 3 + 2HCl → FeCl 2 + H 2 O + CO 2
Tính % khối lượng: Gọi số mol Fe, FeO, FeCO 3 trong hỗn hợp là x, y, z => x + y + z = 0,25
Theo phương trình hóa học : Số mol H 2 , CO 2 là x, z
![]()
Mặt khác : 56x + 72y + 116z = 21,6
Giải ra ta có:
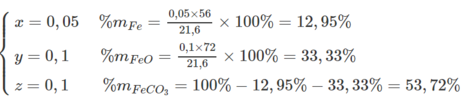

Mong MN giúp mình nhanh với , mình đang rất gấp
Cảm ơn mọi người nhiều nhà 😘😘
a)
Gọi $n_{Fe} = a ; n_{FeO} = b; n_{FeCO_3} = c \Rightarrow 56a + 72b + 116c = 21,6(1)$
$Fe + 2HCl \to FeCl_2 + H_2$
$FeO + 2HCl \to FeCl_2 + H_2O$
$FeCO_3 + 2HCl \to FeCl_2 + CO_2 + H_2O$
\(\dfrac{2a+44c}{a+c}=15.2=30\left(2\right)\)
$n_{FeCl_2} = a + b + c= \dfrac{31,75}{127} = 0,25(3)$
Từ (1)(2)(3) suy ra a = 0,05 ; b = 0,1 ; c = 0,1
$n_{HCl} = 2a + 2b + 2c =0,5(mol)$
$m_{dd\ HCl} = \dfrac{0,5.36,5}{7,3\%} = 250(gam)$
$\%m_{Fe} = \dfrac{0,05.56}{21,6}.100\% = 12,96\%$
$\%m_{FeO} = \dfrac{0,1.72}{21,6}.100\% = 33,33\%$
$\%m_{FeCO_3} = 53,71\%$

Gọi x ,y ,z lần lượt là số mol của Fe , FeO và FeCO3
Ta có các PTHH :
\(\left(1\right)Fe+2HCl\rightarrow FeCl2+H2\uparrow\)
xmol..........2xmol.....xmol........xmol
\(\left(2\right)FeO+2HCl\rightarrow FeCl2+H2O\)
ymol........2ymol.....ymol
\(\left(3\right)FeCO3+2HCl\rightarrow FeCl2+H2O+CO2\)
zmol.............2zmol.............zmol.....................zmol
Theo đề bài ta có : \(\left\{{}\begin{matrix}m\left(mu\text{ối}\right)=mFeCl2=\dfrac{31,75}{127}=0,25\left(mol\right)\\M_{hh-kh\text{í}}=2.15=30\left(\dfrac{g}{mol}\right)\end{matrix}\right.\)
Theo 3 PTHH ta có : nHCl = 2nFeCl2 = 2.0,25 = 0,5 (mol)
a) thể tích dung dịch HCl đã dùng là : \(VHCl=\dfrac{0,5}{0,5}=1\left(lit\right)\)
b) Theo 3 PTHH ta có : nA = n(muối) = 0,25 => nFe + nFeCO3 + nFeO = x + y + z = 0,25 (mol) (1)
Ta có sơ đồ đường chéo sau :
=> \(\dfrac{x}{z}=\dfrac{1}{2}=>z=2x\)
Ta có : \(56x+116y+72z=21,6\left(2\right)\)
Thay z = 2x vào PT 1 và 2 Ta được : \(\left\{{}\begin{matrix}x+y+2x=0,25\left(1\right)\\56x+116y+72.2x=21,6\left(2\right)\end{matrix}\right.\) <=> \(\left\{{}\begin{matrix}3x+y=0,25\\200x+116y=21,6\end{matrix}\right.=>\left\{{}\begin{matrix}x=0,05\\y=0,1\end{matrix}\right.\) => z = 2.0,05 = 0,1
=> \(\left\{{}\begin{matrix}nFe=0,05\left(mol\right)\\nFeCO3=0,1\left(mol\right)\\nFeO=0,1\left(mol\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}\%mFe=\dfrac{0,05.56}{21,6}.100\%\approx12,96\%\\\%mFeO=\dfrac{0,1.72}{21,6}.100\%\approx33,33\%\\\%mFeCO3=100\%-12,96\%-33,33\%=53,71\%\end{matrix}\right.\)
Vậy...................

\(n_{H2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,03 0,06 0,03 0,03
\(MgO+2HCl\rightarrow MgCl_2+H_2O|\)
1 2 1 1
0,03 0,06 0,03
a) \(n_{Mg}=\dfrac{0,03.1}{1}=0,03\left(mol\right)\)
\(m_{Mg}=0,03.24=0,72\left(g\right)\)
\(m_{MgO}=1,92-0,72=1,2\left(g\right)\)
b) Có : \(m_{MgO}=1,2\left(g\right)\)
\(n_{MgO}=\dfrac{1,12}{40}=0,03\left(mol\right)\)
\(n_{HCl\left(tổng\right)}=0,06+0,06=0,12\left(mol\right)\)
400ml = 0,4l
\(C_{M_{ddHCl}}=\dfrac{0,12}{0,4}=0,3\left(l\right)\)
c) \(n_{MgCl2\left(tổng\right)}=0,03+0,03=0,06\left(mol\right)\)
\(C_{M_{MgCl2}}=\dfrac{0,06}{0,4}=0,15\left(M\right)\)
Chúc bạn học tốt

Gọi nFe=a
.......nFeCO3=b
.......nFeO=c
Fe + 2 HCl ➜ FeCl2 + H2
a.........2a............a..........a........(mol)
FeCO3 + 2HCl ➜FeCl2 +CO2 + H2O
b................2b............b..........b........b.....(mol)
FeO + HCl ➜FeCl2 + H2O
c...........2c...........c..........c........(mol)
Ta có các hệ phương trình sau
56a + 116b + 72c = 21.6
a+b=\(\dfrac{3.36}{22.4}=0.15 \)
\(\dfrac{2a+44b}{a+b}=15*2\)
giải 3 phương trình trên ta được
a=0.05;b=0.1;c=0.1
a)mFe=0.05*56=2.8(g)
mFeO=0.1*72=7.2(g)
mFeCO3=0.1*116=11.6(g)
b) m muối = (0.05+0.1+0.1)*127=31.75(g)
c)V=\(\dfrac{0.1+0.2+0.2}{0.5}=1(l)\)

a/ Fe + 2HCl \(\rightarrow\) FeCl2 + H2
nH2 = \(\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Theo PTHH: nH2 = nFe = 0,15 (mol) \(\Rightarrow m_{Fe}=0,15.56=8,4\left(g\right)\)
\(\Rightarrow m_{Cu}=11-8,4=2,6\left(g\right)\)
\(\Rightarrow\%m_{Fe}=\dfrac{8,4}{11}.100\%\approx76,4\%\)
\(\Rightarrow\%m_{Cu}=100-76,4\approx23,6\%\)
b/ Theo PTHH ta có: nHCl = 2nFe = 2.0,15 = 0,3 (mol)
\(\Rightarrow V_{ddHCl}=\dfrac{0,3}{2}=0,15\left(M\right)\)
c/ mHCl = 36,5 . 0,3 = 10,95(g)
\(\Rightarrow C\%_{HCl}=\dfrac{m_{HCl}}{m_{ddHCl}}.100\%=\dfrac{10,95}{200}.100\%=5,475\%\)
Phương trình hóa học: Fe+2HCl→FeCl2+H2
FeO+2HCl→FeCl2+H2
FeCO3+2HCl→FeCl2+H2O+CO2
a) Tính thể tích dung dịch HCl: nHCl=2nFeCl2=2 x 31,75/127 = 0,5(mol)
→VHCl=0,5/0,5 = 1(l)
b) Tính % khối lượng: Gọi số mol Fe, FeO, FeCO3 trong hỗn hợp là x, y, z
=> x + y + z =0,25
Theo phương trình hóa học: Số mol H2 , CO2 là x, z
→¯M=(2x+44z)/(x+z) = 15×2 →z=2x
Mặt khác: 56x + 72y + 116z =21,6
Giải ra ta có: x = 0,05; y = 0,1 và z = 0,
Vậy
%mFe = 0,05 × 56/21,6 × 100% = 12,95%
%mFeO = 0,1 × 72/21,6 × 100% = 33,33%
%mFeCO3 = 100% − 12,95% − 33,33% = 53,72%