Trong tự nhiên đồng có 2 đồng vị 63Cu và 65Cu. Trong đó 65Cu chiếm 27% số nguyên tử .
a) Tính phần trăm khối lượng 65Cu trong tự nhiên
b) Tính phần trăm khối lượng 63Cu trong phân tử Cu2O biết \( \overline{M}\)O = 16
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đồng vị \(^{65}Cu\) chiếm 27% về số nguyên tử.
\(\Rightarrow\)Đồng vị \(^{63}Cu\) chiếm 73% về số nguyên tử.
Số nguyên tử khối:
\(\overline{A_{Cu}}=\dfrac{65\cdot27+63\cdot73}{100}=63,54\)
\(\%m_{^{63}Cu}=\dfrac{63\cdot0,73}{63,54+2\cdot35,5}\cdot100\%=34,18\%\)

Đáp án D
Phần trăm nguyên tử 63Cu trong tự nhiên là: %63Cu = 100 - 27 = 73%.
Khối lượng nguyên tử trung bình của Cu là:
MCu = 65 x 0,27 + 63 x 0,73 = 63,54
Phần trăm của 63Cu trong CuSO4.5H2O là
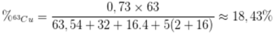

Đáp án B
Giả sử % nguyên tử 65Cu và 63Cu trong tự nhiên lần lượt là x, y.
Ta có hpt:
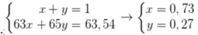
Phần trăm khối lượng của 63Cu trong Cu2O là
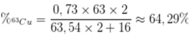

`a)`
\(\%m_{^{65}Cu}=100-73=27\%\)
`->M_{Cu}={63.73+65.27}/{100}=63,54(g//mol)`
`n_{Cu_2O}={7,154}/{63,54.2+16}=0,05(mol)`
`->n_{Cu}=0,1(mol)`
\(\to m_{^{63}Cu}=0,1.63,54.73\%=4,63842(g)\)
`b)`
`\%m_{Cu}={63,54}/{63,54+32+16.4}.100\%\approx 39,827\%`

Đáp án A
Giả sử % nguyên tử 65Cu và 63Cu trong tự nhiên lần lượt là x, y.
Ta có hpt:
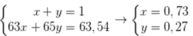
Phần trăm khối lượng của 63Cu trong CuSO4 là
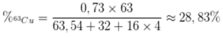
a/ \(\overline{A}_{Cu}=\frac{a_1.A_1+a_2.A_2}{a_1+a_2}=\frac{73\%.63+27\%.65}{100\%}=63,54\)
Xét trong 1(mol) của Cu trong tự nhiên:
\(m_{Cu}\) = n.M = 1.63,54 = 63,54
Có: \(n_{^{65}Cu}=n_{Cu}=1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}^{63}Cu\left(73\%\right)=0,73\left(mol\right)\\^{65}Cu\left(27\%\right)=0,27\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{^{65}Cu}=n.M=0,27.65=17,55\left(g\right)\\m_{^{63}Cu}=n.M=0,73.63=45,99\left(g\right)\end{matrix}\right.\)
Phần trăm khối lượng của \(^{65}Cu\) trong tự nhiên là:
\(\%^{65}Cu_{\left(Cu\right)}=\frac{m_{^{65}Cu}}{m_{Cu}}.100\%=\frac{17,55}{63,54}.100\%\approx27,62\%\)
b/ Có: \(n_{Cu}=2n_{Cu_2O}=1\)
\(\Rightarrow n_{Cu_2O}=0,5\left(mol\right)\)
\(m_{Cu_2O}=n.M=0,5.\left(64.2+16\right)=72\left(g\right)\)
Phần trăm khối lượng \(^{63}Cu\) trong phân tử \(Cu_2O\) là:
\(\%^{63}Cu_{\left(Cu_2O\right)}=\frac{m_{^{63}Cu}}{m_{Cu_2O}}.100\%=\frac{45,99}{72}.100\%=63,875\%\)