Oxit B có công thức là X2O. Tổng số hạt cơ bản trong B là 92, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 28. Biết 168O. Tìm B
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi số hạt mang điện là 2Z, số hạt không mang điện là N
Ta có: \(\left\{{}\begin{matrix}2Z_{\left(phân.tử\right)}+N_{\left(phân.tử\right)}=92\\2Z_{\left(phân.tử\right)}-N_{\left(phân.tử\right)}=28\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}Z_{\left(phân.tử\right)}=30\\N_{\left(phân.tử\right)}=32\end{matrix}\right.\)
Mà \(p_{Oxi}=n_{Oxi}=e_{Oxi}=8\) \(\Rightarrow\left\{{}\begin{matrix}p_X=e_X=\dfrac{30-8}{2}=11\\n_X=\dfrac{32-8}{2}=12\end{matrix}\right.\)
X là Natri

29. Hợp chất A có công thức: X3Y2 có tổng số hạt cơ bản là 150 trong đó tổng số hạt mang điện nhiều hơn số hạt không mang điện là 50. CT của A là A. Ca3N2 B. Mg3N2 C. Ca3P2 D. Mg3P2
---
\(\left\{{}\begin{matrix}6P_X+4P_Y-\left(3N_X+2N_Y\right)=50\\6P_X+4P_Y+3N_X+2N_Y=150\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}6P_X+4P_Y=100\\3N_X+2N_Y=50\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}3P_X+2P_Y=50\\3N_X+2N_Y=50\end{matrix}\right.\\ \Leftrightarrow P_X+P_Y=N_X+N_Y\\ \)
Xét thấy chỉ có trường hợp: PX=12 =NX; PY=7=NY là thỏa mãn
=> Chọn B
30. Hợp chất B có công thức: X2Y có tổng số hạt cơ bản là 140 trong đó tổng số hạt mang điện nhiều hơn số hạt
không mang điện là 44. Số hạt mang điện trong nguyên tử M nhiều hơn trong nguyên tử Y là 22. CT của B là
A. Na2O B. Na2S C. K2O D. K2S
---
\(\left\{{}\begin{matrix}4P_X+2P_Y+2N_X+N_Y=140\\4P_X+2P_Y-\left(2N_X+N_Y\right)=44\\2P_X-2P_Y=22\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}4P_X+2P_Y+2N_X+N_Y=140\\4P_X+2P_Y-\left(2N_X+N_Y\right)=44\\P_X=11+P_Y\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}4P_X+2P_Y=92\\2N_X+N_Y=52\\P_X=11+P_Y\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}44+6P_Y=92\\2N_X+N_Y=52\\P_X=P_Y+11\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}P_Y=Z_Y=8\\P_X=Z_X=19\end{matrix}\right.\)
=> X là Kali còn Y là Oxi
-> CTHH K2O

ông ơi tôi không hiểu sao 2phtrinh 2po no đều mất vậy

Tổng số hạt cơ bản (p, n, e) trong X là 92 → 2. (2pR + nR) + 2pO + nO = 92 → 2. (2pR + nR) = 68
Số hạt mang điện nhiều hơn số hạt không mang điện là 28 → (2.2pR +2.nO )- (2nR + nO) = 28
→ 4pR - 2nR = 20
Giải hệ → pR= 11, nR = 12 → R là Na
Vậy công thức của X là Na2O.
Đáp án B.

Đáp án B
Tổng số hạt cơ bản (p, n, e) trong X là 92
→ 2. (2pR + nR) + 2pO + nO = 92
→ 2. (2pR + nR) = 68
Số hạt mang điện nhiều hơn số hạt không mang điện là 28
→ (2.2pR +2.nO )- (2nR + nO) = 28
→ 4pR - 2nR = 20
Giải hệ → pR= 11, nR = 12 → R là Na

\(\Rightarrow X_2=66-24=42\)
\(\Rightarrow X=21\)
\(\Rightarrow2p_X+n_X=21\left(1\right)\)
\(4p_X+16-2n_X-8=22\)
\(\Leftrightarrow4p_X-2n_X=14\)
\(\Rightarrow2p_X-n_X=7\left(2\right)\)
Từ 1, 2 suy ra :
\(4p_X=28\)
\(\Rightarrow p_X=7\)
-> Nito (N)
-> N2O

a) CT oxit : R2O
\(\left\{{}\begin{matrix}2\left(2Z_R+N_R\right)+2.8+8=140\\4Z_R+8.2-\left(2N_R+8\right)=44\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}Z_R=19\\N_R=20\end{matrix}\right.\)
Vì ZR =19 => R là K
=> Oxit cần tìm là K2O
b) \(n_{K_2O}=0,2\left(mol\right)\)
\(K_2O+H_2O\rightarrow2KOH\)
\(n_{KOH}=2n_{K_2O}=0,4\left(mol\right)\)
=> \(C\%_{KOH}=\dfrac{0,4.56}{18,8+181,2}.100=11,2\%\)


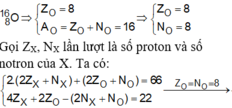
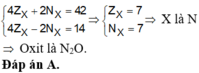
\(\left\{{}\begin{matrix}2\left(2p_X+n_X\right)+2p_O+n_O=92\\2.2p_X+2p_O-2n_X-n_O=28\end{matrix}\right.\)
⇔\(\left\{{}\begin{matrix}4p_X+2n_X+2.8+8=92\\4p_X+2.8-2n_X-8=28\end{matrix}\right.\)
⇔\(\left\{{}\begin{matrix}2p_X+n_X=34\\2p_X-n_X=10\end{matrix}\right.\)
⇔\(\left\{{}\begin{matrix}p_X=11\\n_X=12\end{matrix}\right.\)
⇒X là Na
⇒B là Na2O
Tổng số hạt trong phân tử là 66 => Số hạt trong nguyên tử X là (66-24):2=21 => 2pX +nX=21 (1)
4pX+2pO- 2nX-nO=22 => 2pX - nX= 7 (2)
Từ (1) và (2) ta có hệ phương trình, giải hệ phương trình ta tìm được pX= 7
nX=7
Vậy X là N
Công thức oxit là N2O