Hỗn hợp x gồm CH4 và hiđrocacbon a với tỉ lệ số mol tương ứng trong hỗn hợp là 2:1 đốt cháy hoàn toàn 6,72 lít hỗn hợp A thu được 22 gam khí CO2 và 14,4 gam H2O hãy xác định công thức cấu tạo của A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Khi cho hỗn hợp A qua dung dịch brom dư, có phản ứng :
C 2 H 2 + 2 Br 2 → C 2 H 2 Br 4
Vì phản ứng xảy ra hoàn toàn và có hai khí thoát ra khỏi dung dịch brom, nên hai khí đó là CH 4 và C n H 2 n + 2
Theo đề bài V C 2 H 2 tham gia phản ứng là : 0,896 - 0,448 = 0,448 (lít).
Vậy số mol C 2 H 2 là 0,448/22,4 = 0,02 mol
Gọi số mol của CH 4 là X. Theo bài => số mol của C n H 2 n + 2 cũng là x.
Vậy ta có : x + x = 0,448/22,4 = 0,02 => x = 0,01
Phương trình hoá học của phản ứng đốt cháy hỗn hợp :
2 C 2 H 2 + 5 O 2 → 4 CO 2 + 2 H 2 O
CH 4 + 2 O 2 → CO 2 + 2 H 2 O
2 C n H 2 n + 2 + (3n+1) O 2 → 2n CO 2 + 2(n+1) H 2 O
Vậy ta có : n CO 2 = 0,04 + 0,01 + 0,01n = 3,08/44 => n = 2
Công thức phân tử của hiđrocacbon X là C 2 H 6

Tính % thể tích các khí :
% V C 2 H 2 = 0,448/0,896 x 100% = 50%
% V CH 4 = % V C 2 H 6 = 25%

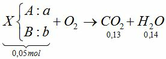
Đốt cháy ankin => nCO2 > nH2O mà theo bài ra nCO2 < nH2O
=> B là ankan nCO2 < nH2O
Nhận xét:
Đốt ankin: – nankin = nH2O – nCO2
Đốt ankan: nankan = nH2O – nCO2
=> b – a = 0,01 và b + a = 0,05
=> a = 0,02 và b = 0,03
=> số C trung bình = 2,6 và số H trung bình = 5,6
TH1: số C trong ankin < 2,6 => A là C2H2: 0,02 và B: 0,03
=> B: 44 (C3H8)
TH2: số C trong ankan < 2,6 => A : 0,02 và CH4: 0,03
=> A: 68 (C5H8) loại do hh khí
TH3: số C trong ankan < 2,6 => A: 0,02 và C2H6: 0,03
=> A: 47 (lẻ) => loại
Vậy A là C2H2 (axetilen/ etin) và B là C3H8 (propan)

Đáp án A
Hỗn hợp chứa axetilen, etilen và chất A khi đốt thu được CO2 và H2O tỉ lệ 1:1 thì chất A chắc chắn phải là ankan (do axetilen đốt thu được nCO2 > nH2O, etilen đốt thu được nCO2=nH2O, cần phải có 1 chất đốt thu được nCO2< nH2O để đảm bảo tỉ lệ)
Hơn nữa, nC2H2=nA
Khí thoát ra khỏi bình là ankan:
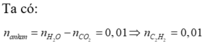
Khối lượng bình tăng lên là khối lượng của axetilen và etilen.


Ta có nCO2 = 0,5; nH2O = 0,6; nhỗn hợp = 0,3 Số C trung bình = 0,5/0,3 = 1,67
=>X là CH4
=>Chọn C.

Đáp án C
Ta có nCO2 = 0,5; nH2O = 0,6; nhỗn hợp = 0,3
Số C trung bình = 0,5/0,3 = 1,67
X là CH4

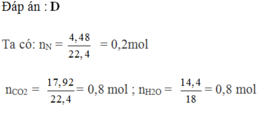
Ta thấy: nH2O = nCO2 => hidrocacbon N là anken
CnH2n + O2 à nCO2 + nH2O
0,2 0,8
=> 0,2n = 0,8 => n = 4 => anken là C4H8
=> N, P, Q là các đồng phân của nhau và cùng CTPT là C4H8
Khi đốt cháy N hoặc P hoặc Q đều cho số mol CO2 và H2O giống nhau
CH3-CH2-CH2-CH3 (1) CH3-CH(CH3)-CH3 (2)
Trong 2 đồng phân trên chỉ có (1) tách hidro cho 3 sản phẩm là đồng phân của nhau
CH3-CH2-CH2-CH3 à CH3-CH=CH-CH3 + H2
(cis-trans)
CH3-CH2-CH2-CH3 à CH2=CH-CH2-CH3 + H2

Chọn đáp án C
♦ giải đốt 33 , 3 g a m E + O 2 → t 0 1 , 35 m o l C O 2 + 1 , 35 m o l H 2 O
Tương quan n C O 2 = n H 2 O
⇒ hai este là đồng phân của este no, đơn chức, mạch hở.
mE = mC + mH + mO
⇒ nE = 1 2 nO trong E = 0,45 mol
⇒ số C = 1,35 ÷ 0,45 = 3
⇒ 2 este đồng phân C3H6O2 là HCOOC2H5 và CH3COOCH3.
♦ thủy phân: 33 , 3 g a m E ( 0 , 45 m o l ) + 0 , 6 m o l N a O H → 38 , 7 g a m r ắ n k h a n T + a n c o l
⇒ giải hỗn hợp T gồm 0,15 mol NaOH dư, 0,3 mol HCOONa và 0,15 mol CH3COONa.
⇒ đốt T thu được 0 , 3 m o l N a 2 C O 2 + 0 , 3 m o l C O 2 + 0 , 45 m o l H 2 O
⇒ Yêu cầu n C O 2 : n H 2 O = 0 , 3 : 0 , 45 = 2 : 3

Ta có:
\(n_{hh}=\frac{6,72}{22,4}=0,3\left(mol\right)\)
\(\Rightarrow n_{CH4}=0,2\left(mol\right);n_A=0,1\left(mol\right)\)
\(X+O_2\rightarrow CO_2+H_2O\)
\(n_{CO2}=\frac{22}{44}=0,5\left(mol\right)\)
\(n_{H2O}=\frac{14,4}{18}=0,8\left(mol\right)\)
\(\Rightarrow n_{H2O}-n_{CO2}=n_X\)
Vậy hidrocacbon A cũng là ankan có dạng CnH2n+2
\(\Rightarrow0,2.1+0,1.n=0,5\)
\(\Rightarrow n=3\)
Suy ra A là C3H8
CTCT: CH3−CH2−CH3