Cho sơ đồ phản ứng sau:
NaOH+FeCl3→NaCl+Fe(OH)3
Biết có 6 g NaOH đã được cho vào dung dịch chứa 32,5g FeCl3, khuấy đều
a, chất nào dư sau phản ứng,dư bao nhiêu g
b, tính khối lượng kết tủa thu được
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: \(3NaOH+FeCl_3\rightarrow3NaCl+Fe\left(OH\right)_3\downarrow\)
Ta có: \(n_{NaOH}=\dfrac{10}{40}=0,25\left(mol\right)\)
\(\Rightarrow n_{FeCl_3}=n_{Fe\left(OH\right)_3}=\dfrac{1}{12}\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}m_{FeCl_3}=\dfrac{1}{12}\cdot162,5\approx13,54\left(g\right)\\m_{Fe\left(OH\right)_3}=\dfrac{1}{12}\cdot107\approx8,92\left(g\right)\end{matrix}\right.\)
nNaOH = m/M = 10/(23 +16 + 1) = 0,25 (mol)
Ta có PTHH: 3NaOH + FeCl3 ------> Fe(OH)3 + 3NaCl
Theo PT: 3 - 1 - 1 (mol)
BC: 0.25 - 0.083 - 0.083 (mol)
Suy ra: mFeCl3 = n x M = 0.083 x (56 + 35,5 x 3) = 13,4875 (g)
mFe(OH)3 = n x M = 0,083 x (56+17 x 3) = 8,881 (g)

Đáp án A
Chất rắn B nguyên chất nên B là Cu
=> Fe và Zn phản ứng hết.
G là ZnO


số mol NaOH là:\(n_{NaOH}=\frac{10}{23+16+1}=0,25\left(mol\right)\)
PTHH\(3NaOH+FeCl_3\rightarrow Fe\left(OH\right)_3+3NaCl\)
\(m_{FeCl_3}=n.M=\frac{0.25}{3}\cdot\left(56+35,5\cdot3\right)\approx13,54\left(g\right)\)
\(m_{Fe\left(OH\right)_3}=n.M=\frac{0.25}{3}\cdot\left(56+\left(16+1\right)\cdot3\right)\approx8,91\left(g\right)\)
\(m_{NaCl}=n.M=0.25\cdot\left(23+35.5\right)=14.625\left(g\right)\)

Đáp án D
Ta có: n FeCl 3 = 0 , 16 ; n CuCl 2 = 0 , 12
Cho AgNO3 dư vào X thu được kết tủa gồm AgCl 0,72 mol (bảo toàn nguyên tố Cl) và Ag 0,06 mol.
Nếu cho NaOH dư vào X thì lượng NaOH phản ứng 0,78 mol, do vậy
n Al = 0 , 78 - 0 , 72 = 0 , 06 mol
Do n Ag = 0 , 06 → n Fe + 2 trong X = 0 , 06 mol
Ta có: n Fe 2 + < n FeCl 3 và khối lượng rắn tăng do vậy Fe dư
Gọi số mol Mg là a mol, Fe là b mol
→ m = 24a+56b+0,06.27
Rắn Y sẽ chứa Cu 0,12 mol và Fe 0,1+b mol
→ 1,8275m = 0,12.64+56(0,1+b)
Dung dịch X chứa MgCl2 a mol, AlCl3 0,06 mol và FeCl2 0,06 mol
→ a = 0 , 72 - 0 , 06 . 3 - 0 , 06 . 2 2 = 0,21 mol → b = 67 2800
→ m = 8 gam

Đáp án D
Ta có: ![]()
Cho AgNO3 dư vào X thu được kết tủa gồm AgCl 0,72 mol (bảo toàn nguyên tố Cl) và Ag 0,06 mol.
Nếu cho NaOH dư vào X thì lượng NaOH phản ứng 0,78 mol, do vậy
![]()
Do n A g = 0 , 06 m o l → n F e 2 + t r o n g X = 0 , 06 m o l
Ta có: n F e 2 + < n F e C l 3 và khối lượng rắn tăng do vậy Fe dư
Gọi số mol Mg là a mol, Fe là b mol
=> m = 24a + 56b + 0,06.27
Rắn Y sẽ chứa Cu 0,12 mol và Fe 0,1+b mol
=> 1,8275m = 0,12.64 + 56(0,1+b)
Dung dịch X chứa MgCl2 a mol, AlCl3 0,06 mol và FeCl2 0,06 mol
![]()
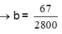
=> m = 8 gam

Đáp án D
Ta có:
n F e C l 3 = 0 , 16 ; n C u C l 2 = 0 , 12
Cho AgNO3 dư vào X thu được kết tủa gồm AgCl 0,72 mol (bảo toàn nguyên tố Cl) và Ag 0,06 mol.
Nếu cho NaOH dư vào X thì lượng NaOH phản ứng 0,78 mol, do vậy
n A l = 0 , 78 - 0 , 72 = 0 , 06 m o l
Do n A g = 0 , 06 → n F e + 2 t r o n g X = 0 , 06 m o l
Ta có: n F e 2 + < n F e C l 3 và khối lượng rắn tăng do vậy Fe dư
Gọi số mol Mg là a mol, Fe là b mol
→ m = 24 a + 56 b + 0 , 06 . 27
Rắn Y sẽ chứa Cu 0,12 mol và Fe 0,1+b mol
→ 1 , 8275 m = 0 , 12 . 64 + 56 ( 0 , 1 + b )
Dung dịch X chứa MgCl2 a mol, AlCl3 0,06 mol và FeCl2 0,06 mol
![]()
→ b = 67 2800
→ m = 8 g a m

Chất rắn thu được sau khi nung là ZnO.
\(\Rightarrow n_{ZnO}=\dfrac{8,1}{81}=0,1\left(mol\right)\)
BTNT Zn, có: nZn = nZnO = 0,1 (mol)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{0,1.65}{13,5}.100\%\approx48,15\%\\\%m_{Fe}\approx100-48,15=51,85\%\end{matrix}\right.\)
a) nNaOH= 6/40=0,15(mol)
nFeCl3=32,5/162,5= 0,2(mol)
PTHH: 3 NaOH + FeCl3 -> Fe(OH)3 + 3 NaCl
0,15________0,05____0,05________0,15(mol)
Ta có: 0,2/1 > 0,15/3
=> NaOH hết, FeCl3 dư
=> nFeCl3(dư)= 0,2-0,05=0,15(mol)
=> mFeCl3= 162,5.0,15=24,375(g)
b)m(kết tủa)= mFe(OH)3= 0,05.107= 5,35(g)
cảm ơn nhiều ạ