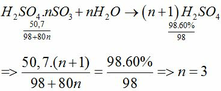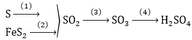6. Khi hấp thụ SO3 vào dd H2SO4 đặc , người ta thu đc một loại oleum có công thức H2SO4.nSO3. Biết rằng trong loại oleum trên chứa 36,7% về khối lượng là nguyên tố lưu huỳnh. Công thức của loại oleum trên là?
9. Một loại oleum có công thức H2SO4.nSO3 . Biết rằng trong loại oleum trên chứa 55,05% về khối lượng là SO3. Công thức của loại oleum trên là?