Một loại khí X có chứa 2 đồng vị 3517X, 3717X. Cho X2 tác dụng với H2 rồi lấy sản phẩm hoà tan vào nước thu được dung dịch Y. Chia dung dịch Y thành hai phần bằng nhau:
- Phần thứ nhất cho tác dụng vừa đủ với 125 ml dung dịch Ba(OH)2 0,88M.
- Phần thứ hai cho tác dụng với AgNO3 vừa đủ ta thu được 31,57 gam kết tủa.
Thành phần % số nguyên tử của mỗi đồng vị là bao nhiêu?
A. 35 và 65
B. 40 và 60
C. 85 và 15
D. 75 và 25


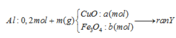
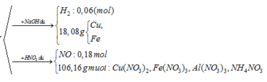
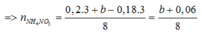





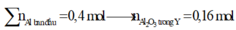
Đáp án D
Gọi phần trăm số nguyên tử của X 17 35 là x, X 17 37 là (100 – x).
Vậy thành phần phần trăm mỗi loại đồng vị của clo là : C 17 35 l (75% ) ; C 17 37 l (25%).