Cho 2,4 lít khí H 2 tác dụng với 7,6 lít khí O 2 thu được khối lượng nước là? Biết các thể tích khí được đo ở đktc.
A. 1,92g
B. 1,93g
C. 4,32g
D. 0,964g
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H_2}=\dfrac{V}{22,4}=\dfrac{4,958}{22,4}=\approx0,2\left(mol\right)\)
\(n_{O_2}=\dfrac{V}{22,4}=\dfrac{1,2395}{22,4}\approx0,05\left(mol\right)\)
\(PTHH:2H_2+O_2\rightarrow2H_2O\)
Ta có: \(\dfrac{n_{H_2}}{2}=\dfrac{0,2}{2}=0,1>\dfrac{n_{O_2}}{1}=\dfrac{0,05}{1}=0,05\)
→ Sau pư O2 hết, H2 dư
→ Theo \(n_{O_2}\)
Theo PTHH \(n_{H_2O}=2n_{O_2}=2.0,05=0,1\left(mol\right)\)
\(V_{H_2O\left(đktc\right)}=n.22,4=0,1.22,4=2,24\left(l\right)\)
Vậy ...

Số mol của 4,48 lít H2:
\(n_{H_2}=\dfrac{V}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH:
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
tỉ lệ: 2 : 1 : 2
0,2-> 0,1 : 0,2( mol)
a/ số gam của 0,2 mol nước:
\(m_{H_2O}=n.M=0,2.=3,6\left(g\right)\)
b/ thể tích của 0,1 mol khí O2:
\(V_{O_2}=n.22,4=0,1.22,4=2,24\left(l\right)\)

Bài 1:
PTHH: \(CH_4+Cl_2\underrightarrow{a/s}CH_3Cl+HCl\)
Theo PTHH: \(n_{Cl_2}=n_{CH_3Cl}=n_{CH_4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{CH_3Cl}=0,15\cdot50,5=7,575\left(g\right)\\V_{CH_4}=V_{Cl_2}=3,36\left(l\right)\end{matrix}\right.\)
Bài 2:
PTHH: \(CH_4+2O_2\underrightarrow{a/s}CO_2+2H_2O\)
Theo PTHH: \(\left\{{}\begin{matrix}n_{CO_2}=n_{CH_4}\\n_{O_2}=2n_{CH_4}\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{CO_2}=V_{CH_4}=5,6\left(l\right)\\V_{CO_2}=2V_{CH_4}=11,2\left(l\right)\end{matrix}\right.\)

Bài 5
nH2=V22,4=22,422,4=1(mol)nH2=V22,4=22,422,4=1(mol)
nO2=V22,4=16,822,4=0,75(mol)nO2=V22,4=16,822,4=0,75(mol)
2H2+O2→2H2O2H2+O2→2H2O
Ban đầu : 1 0,75 (mol)
Phản ứng 1 0,5 1 (mol)
Còn lại 0 0,25 1 (mol)
mH2O=1.18=18(g)

\(n_{H_2}=\dfrac{8.4}{22,4}=0,375\left(mol\right)\)
\(n_{O_2}=\dfrac{2.8}{22,4}=0,125\left(mol\right)\)
PTHH : 2H2 + O2 -> 2H2O
0,125 0,25
Ta thấy : 0,375 > 0,125 => H2 dư , O2 đủ
\(m_{H_2O}=0,25.18=4,5\left(g\right)\)
\(n_{H_2}=\dfrac{V_{H_2}}{22,4}=\dfrac{8,4}{22,4}=0,375mol\)
\(n_{O_2}=\dfrac{V_{O_2}}{22,4}=\dfrac{2,8}{22,4}=0,125mol\)
\(2H_2+O_2\rightarrow\left(t^o\right)2H_2O\)
0,375 >0,125 ( mol )
0,125 0,25 ( mol )
\(m_{H_2O}=n_{H_2O}.M_{H_2O}=0,25.18=4,5g\)

Đáp án C.
Cứ 278 g FeSO4.7H2O có 152 g FeSO4
→ 55,6 g FeSO4.7H2O có x (g) FeSO4
Khối lượng FeSO4 là 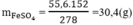
Số mol FeSO4: 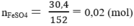
Fe + H2SO4 → FeSO4 + H2
nH2 = nFeSO4 = 0,2 (mol) ⇒ VH2 = 0,2.22,4 = 4,48 (lit)

Có thiếu đề không bạn ? Nếu không cho kim loại cụ thể bài này không làm được!
Đáp án B