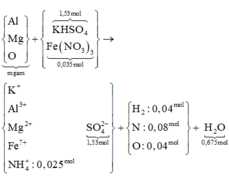
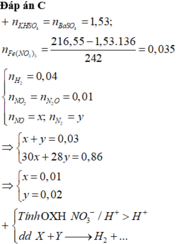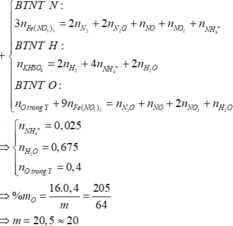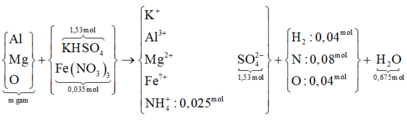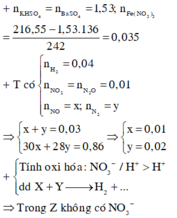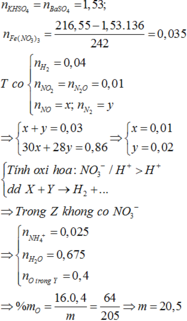Hòa tan hoàn toàn 216,55 gam hỗn hợp K H S O 4 , F e N O 3 3 vào nước được dung dịch X. Cho m gam hỗn hợp Y gồm Mg, Al, MgO và A l 2 O 3 (trong đó oxi chiếm 64/205 về khối lượng) tan hết vào X, sau khi các phản ứng kết thúc thu được dung dịch Z chỉ chứa muối trung hòa và 2,016 lít hỗn hợp khí T có tổng khối lượng 1,84 gam gồm 5 khí (đktc), trong đó về thể tích H 2 , N 2 O , N O 2 lần lượt chiếm 4/9, 1/9 và 1/9. Cho B a C l 2 dư vào Z thu được 356,49 gam kết tủa. Giá trị của m gần nhất với giá trị nào sau đây?
A. 30.
B. 35.
C. 20.
D. 40.