Một nguyên tố thuộc nhóm VIA, chu kỳ 3. Điện tích hạt nhân của nguyên tử nguyên tố đó là:
A. 13+
B. 14+
C. 15+
D. 16+
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Zx+zy=51
Hai nhóm liên kết nhau ở chu kỳ 4
=> TH1: zy-zx=1
=>TH2: zy-zx=11

Đầu tiên là F fluorine số electon 19 stt 9 chu kì 2 nhóm VIIA
Thứ 2 là sodium số electon 23 stt 11 chu kì 3 nhóm IA
Cuối cùng là scandium số electon là 45 stt 21 chu kì 4 nhóm IIIB

B
Cấu hình e của R: 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6 3 d 10 4 s 2 4 p 5
→ p = e = 35. Hạt nhân nguyên tử của nguyên tố R có điện tích 35+

Đáp án D
Hai nguyên tố thuộc cùng một nhóm A, thuộc hai chu kỳ liên tiếp = Điện tích hạt nhân cách nhau 8, 18 hay 32
Trường hợp 1:
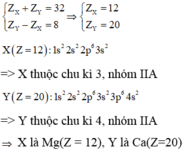
Trường hợp 2:
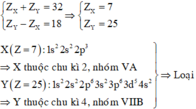
Trường hợp 3:
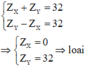

Đáp án C
Theo đề bài, ta có: ZX + ZY = 22 (1)
- Nếu X, Y thuộc hai chu kì nhỏ thì (ZX < ZY): ZY = ZX + 8 (2)
Từ (1) và (2) => ZX =7; ZY = 15.
Vậy X là N, Y là P
- Nếu X thuộc chu kì nhỏ và Y thuộc chu kì lớn thì: ZY = ZX + 18 (3)
Từ (1) và (3) => ZX = 2; ZY = 20 (loại vì không thảo mãn đề bài)
- Nếu X, Y thuộc hai chu kì lớn: ZY = ZX + 32 (4)
Từ (1) và (4) => ZX <0 (loại)

Trong một chu kỳ, theo chiều tăng của điện tích hạt nhân:
- Tuy nguyên tử các nguyên tố có cùng số lớp electron, nhưng khi điện tích hạt nhân tăng, lực hút giữa hạt nhân với các electron lớp ngoài cùng cũng tăng theo, do đó bán kính nói chung giảm dần → Đáp án A sai vì số lớp electron không đổi.
- Lực liên kết giữa hạt nhân và electron lớp ngoài cùng tăng, làm cho năng lượng ion hóa nói chung cũng tăng theo → Đáp án B sai.
- Độ âm điện tăng dần.
- Tính bazơ của oxit và hiđroxit tương ứng giảm dần, đồng thời tính axit của chúng tăng dần → Đáp án C sai.
→ Chọn D.

Tham khảo
ZA + ZB = 32
=> { ZA - ZB = 8 =>{ ZA = 20 -> A là Ca
ZA + ZB = 32 ZB = 12 -> B là Mg
Ca: 1s22s22p63s23p64s2
Mg: 1s22s22p63s2
Đáp án D
Nhóm VIA => có 6 electron lớp ngoài cùng
Chu kì 3 => có 3 lớp eletron
=> Cấu hình electrong: 1s22s22p63s2 p4 => Z=16