Hòa tan hết 2,88g hỗn hợp gồm Fe và Mg trong dd HNO3 loãng, dư thu được 0,9856 lít hỗn hợp khí X gồm NO và N2 ở 27,3 độ C, 1 atm, có tỉ khối so với H2 bằng 14,75.Vậy % theo khối lượng mỗi kim loại trong hỗn hợp bằng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án C:
Gọi x, y là số mol Mg và Fe trong mỗi phần
=> 24x+56y = 4,32
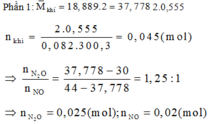

Phần 2: Gọi a, b lần lượt là số mol của AgNO3 và Cu(NO3)2
Sau phản ứng có 3 kim loại là Ag, Cu và Fe dư.
Gọi số mol Fe tham gia phản ứng là t (mol)
Bảo toàn electron ta có: nenhường= ne nhận
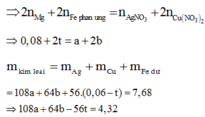
Chỉ có duy nhất Fe dư tan trong HCl
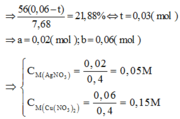

Đáp án D
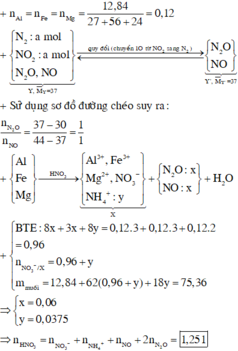
Có : nFe = nAl = nMg = 0,12 mol
Y : N2 ; N2O ; NO và NO2( N2 và NO2 có số mol bằng nhau)
=> Qui đổi : NO2 +N2 -> NO + N2O
=> Y trở thành : NO và N2O với số mol lần lượt là x và y.
Có : MY = 37g => mY = 37(x + y) = 30x + 44y
=> x = y(1)
Giả sử có z mol NH4NO3 trong muối
Bảo toàn e : 3nFe + 3nAl + 2nMg = 3nNO + 8nN2O + 8nNH4NO3
=> 3x + 8y + 8z = 0,96 mol(2)
Và : nHNO3 = (4x + 10y + 10z)
=> nH2O = ½ (nHNO3 – 4nNH4NO3) = (2x + 5y + 3z) mol
Bảo toàn khối lượng :
mY = mKL + mHNO3 – mH2O - mmuối X = (216x + 540y + 576z) – 62,52 = 37(x + y)
=> 179x + 503y + 576z = 62,52(3)
Từ (1),(2),(3) => x = y = 0,06 ; z = 0,0375 mol
=> nHNO3 pứ = 4x + 10y + 10z = 1,215 mol

Đáp án B
- Khi cho hỗn hợp tác dụng với H2SO4 loãng dư chỉ có Mg phản ứng sinh ra khí H2 => nMg=nH2=0,15 mol
- Khi cho hỗn hợp tác dụng với HNO3 dư => Chỉ có Cu và Mg (kim loại thay đổi số oxi hóa)
BT e: nCu=(3nNO-2nMg)/2=0,15 mol
=>mCu=0,15.64=9,6 gam

Có : nFe = nAl = nMg = 0,12 mol
Y : N2 ; N2O ; NO và NO2( N2 và NO2 có số mol bằng nhau)
=> Qui đổi : NO2 +N2 -> NO + N2O
=> Y trở thành : NO và N2O với số mol lần lượt là x và y.
Có : MY = 37g => mY = 37(x + y) = 30x + 44y
=> x = y(1)
Giả sử có z mol NH4NO3 trong muối
Bảo toàn e : 3nFe + 3nAl + 2nMg = 3nNO + 8nN2O + 8nNH4NO3
=> 3x + 8y + 8z = 0,96 mol(2)
Và : nHNO3 = (4x + 10y + 10z)
=> nH2O = ½ (nHNO3 – 4nNH4NO3) = (2x + 5y + 3z) mol
Bảo toàn khối lượng :
mY = mKL + mHNO3 – mH2O - mmuối X = (216x + 540y + 576z) – 62,52 = 37(x + y)
=> 179x + 503y + 576z = 62,52(3)
Từ (1),(2),(3) => x = y = 0,06 ; z = 0,0375 mol
=> nHNO3 pứ = 4x + 10y + 10z = 1,215 mol

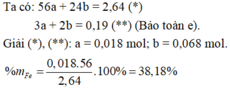

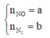

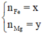
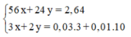
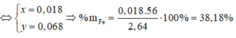

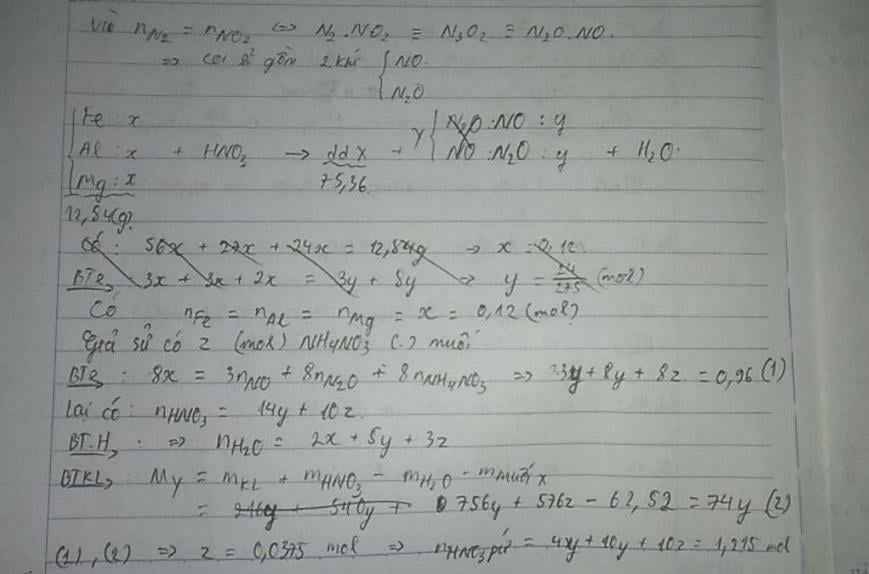
Đặt \(\hept{\begin{cases}x=n_{NO}\\y=n_{N_2}\end{cases}}\)
Sử dụng công thức \(P.V=n.R.T\Leftrightarrow1.0,9856=n.0,082.\left(27,3+273\right)\rightarrow n_{HH}=0,04mol\)
Lập hệ phương trình \(\hept{\begin{cases}x+y=0,04\\30x+28y=14,75.2.0,04\end{cases}}\)
\(\rightarrow\hept{\begin{cases}x=0,03mol\\y=0,01mol\end{cases}}\)
Đặt \(\hept{\begin{cases}a=n_{Fe}\\b=n_{Mg}\end{cases}}\)
Xét sự thay đổi e
\(Fe^0\rightarrow Fe^{+3}+3e\)
\(Mg^0\rightarrow Mg^{+2}+2e\)
\(N^{+5}+3e\rightarrow N^{+2}\)
\(2N^{+5}+10e\rightarrow2N^0\)
Có số mol e nhường = số mol e nhận
\(\Leftrightarrow3.n_{Fe}+2.n_{Mg}=3.n_{NO}+10.n_{N_2}\)
\(\Leftrightarrow3x+2y=3.0,03+10.0,01\)
Lệ hệ phương trình \(\hept{\begin{cases}56x+27y=2,88\\3x+2y=0,19\end{cases}}\)
\(\rightarrow\hept{\begin{cases}x=0,03mol\\y=0,05mol\end{cases}}\)
\(\%m_{Fe}=\frac{0,03.56.100}{2,88}=58,33\%\)
\(\%m_{Mg}=100-58,33=41,67\%\)