Trong tự nhiên, Clo có 2 đồng vị C 35 l và C 37 l , trong đó đồng vị chiếm C 35 l 75% về số đồng vị. Nguyên tử khối trung bình của Cl là
A. 35,54.
B. 35,50.
C. 36,5.
D. 35,6.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(\%^{35}Cl=x\%\Rightarrow\%^{37}Cl=\left(100-x\right)\%\)
\(\overline{M}=\dfrac{35x+37\cdot\left(100\%-x\right)}{100\%}=35.5\left(g\text{/}mol\right)\)
\(\Rightarrow x=75\%\)
\(\%^{37}Cl_{\left(HClO_4\right)}=\dfrac{25\%\cdot37}{1+35.5+16\cdot4}\cdot100\%=9.2\%\)
Phần trăm đồng vị 35Cl = x, thì % đồng vị 37Cl = 100 - x
Ta có:
, vậy x = 75%.
Phần trăm khối lượng của 37Cl trong HClO4=
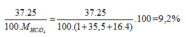

ChọnC
Nguyên tử khối trung bình của Cl là :
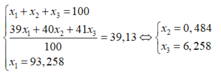
Giả sử có 1 mol K C l O 4 → Số mol Cl = 1; số mol C 35 l là 0,75.
Phần trăm khối lượng của C 35 l trong K C l O 4 là
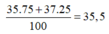

Gọi: x là % nguyên tử \(\frac{35}{17}Cl\) và (100-x ) là % nguyên tử \(\frac{37}{17}Cl\)
Ta có : x + y = 100 (1)
Mặt khác :
\(\overline{M}=\frac{35x+37y}{100}=35.5\)
<=> 35x + 37y = 3550 (2)
Giải (1) và (2) :
x = 75
y = 25
Vậy: \(\frac{37}{17}Cl\) chiếm 25% khối lượng trong phân tử HClO4
Chọn B
Nguyên tử khối trung bình của Cl là :