Cho 3,48 gam bột Mg tan hết trong dung dịch hỗn hợp gồm HCl dư và KNO3, thu được dung dịch X chứa m gam muối và 0,56 lít hỗn hợp khí Y gồm N2 và H2 ở đktc. Khí Y có tỉ khối so với H2 bằng 11,4. Giá trị của m là:
A. 16,085
B. 18,300
C. 14,485
D. 18,035


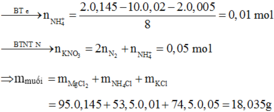
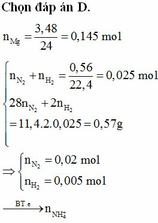

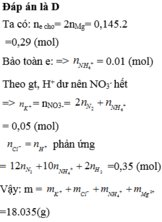



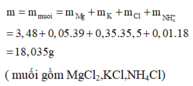

Ta có nMg=0,145 mol
Gọi x và y lần lượt là số mol của H2 và N2
Ta có: x+ y= 0,025; 2x+ 28y= 0,025.(11,4.2) → x= 0,005; y= 0,02
Vì có khí H2 thoát ra → NO3- hết → Muối thu được là muối clorua
QT cho e:
Mg → Mg2++ 2e (1)
0,145→ 0,29 mol
QT nhận e:
2N+5+ 10e →N2 (2)
0,2← 0,02 mol
2H+1+2e→ H2 (3)
0,01← 0,005 mol
Nếu chỉ có quá trình nhận (2) và (3) thì
ne nhận= 0,2+ 0,01= 0,21 mol≠ 0,29 mol
→ Còn có quá trình nhận e tạo muối NH4+
Theo ĐL bảo toàn e: ne cho=n e nhận= 0,29 mol → e nhận ở (4)= 0,29-0,21=0,08 mol
NO3-+ 8e+ 10H+ → NH4++ 3H2O (4)
0,08 → 0, 01 mol
Bảo toàn nguyên tố N ta có
nN(KNO3)= nN(N2)+ nN (NH4+)=2.0,02+ 0,01= 0,05 mol= nKNO3= nK+
Muối chứa Mg2+: 0,145 mol, NH4+: 0,01 mol, K+: 0,05 mol, Cl-
Dùng bảo toàn điện tích: 0,145.2+ 0,01.1+ 0,05= nCl-= 0,35 mol
→mmuối=m= 0,145.24+ 0,01.18+ 0,05.39+ 0,35.35,5= 18,035 gam
Đáp án D