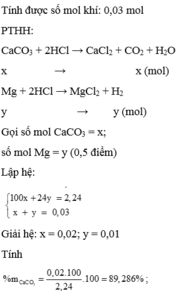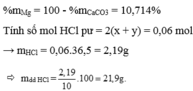Cho 73 gam dung dịch HCl 15% tác dụng vừa đủ với a gam CaCO3, thu được dung dịch A và khí B. Tính khối lượng và số mol HCl sau phản ứng? Tính khối lượng a g CaCO3 cần dùng? Xác định dung dịch A và khí B? Tính nồng độ % (C%) của dung dịch A sau phản ứng?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) \(m_{HCl}=\dfrac{200.10,95}{100}=21,9\left(g\right)\)
=> \(n_{HCl}=\dfrac{21,9}{36,5}=0,6\left(mol\right)\)
b) \(n_{CaCO_3}=\dfrac{a}{100}=0,01a\left(g\right)\)
\(n_{NaOH}=0,05.2=0,1\left(mol\right)\)
PTHH: CaCO3 + 2HCl --> CaCl2 + CO2 + H2O
______0,01a---->0,02a---->0,01a->0,01a___________(mol)
NaOH + HCl --> NaCl + H2O
_0,1----->0,1___________________________________(mol)
=> 0,02a = 0,6 - 0,1
=> a = 25 (g)
c) \(V_{CO_2}=0,01.25.22,4=5,6\left(l\right)\)
d) \(\left\{{}\begin{matrix}C\%\left(CaCl_2\right)=\dfrac{0,25.111}{25+200-0,25.44}.100\%=12,97\%\\C\%\left(HCl_{dư}\right)=\dfrac{0,1.36,5}{25+200-0,25.44}.100\%=1,705\%\end{matrix}\right.\)

PTHH: \(K_2SO_3+2HCl\rightarrow2KCl+H_2O+SO_2\uparrow\)
a+b+c) Ta có: \(n_{SO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{KCl}=0,5\left(mol\right)=n_{HCl}\\n_{K_2SO_3}=0,25\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{K_2SO_3}=0,25\cdot158=39,5\left(g\right)=a\\m_{KCl}=0,5\cdot74,5=37,25\left(g\right)\\m_{ddHCl}=\dfrac{0,5\cdot36,5}{10,95\%}\approx166,67\left(g\right)\end{matrix}\right.\)
Mặt khác: \(m_{SO_2}=0,25\cdot64=16\left(g\right)\)
\(\Rightarrow m_{dd}=m_{K_2SO_3}+m_{ddHCl}-m_{SO_2}=190,17\left(g\right)\) \(\Rightarrow C\%_{KCl}=\dfrac{37,25}{190,17}\cdot100\%\approx19,59\%\)
d) PTHH: \(NaOH+HCl\rightarrow NaCl+H_2O\)
Theo PTHH: \(n_{NaOH}=n_{HCl}=0,5\left(mol\right)\) \(\Rightarrow V_{NaOH}=\dfrac{0,5}{0,5}=1\left(l\right)\)

\(n_{Fe}=\dfrac{11.2}{56}=0.2\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(0.2......0.4...........0.2.......0.2\)
\(m_{FeCl_2}=0.2\cdot127=25.4\left(g\right)\)
\(m_{HCl}=0.4\cdot36.5=14.6\left(g\right)\)
\(V_{H_2}=0.2\cdot22.4=4.48\left(l\right)\)
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
Khí a là Hidro
Ta có: \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{HCl}=0,4mol\\n_{FeCl_2}=n_{H_2}=0,2mol\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{HCl}=0,4\cdot36,5=14,6\left(g\right)\\m_{FeCl_2}=0,2\cdot127=25,4\left(g\right)\\V_{H_2}=0,2\cdot22,4=4,48\left(l\right)\end{matrix}\right.\)