Thủy phân hoàn toàn 20,4 gam phenyl axetat trong 400 ml dung dịch KOH 1M, cô cạn dung dịch sau phản ứng thu được m gam rắn. Giá trị của m là
A. 40,1.
B. 34,5.
C. 39,2.
D. 33,7.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn đáp án C
nCH3COOC6H5 = 5,44/136 = 0,04 và nCH3COOCH2C6H5 = 18/150 = 0,12
⇒ nKOH phản ứng tối đa = 0,04.2 + 0,12 = 0,2 < 0,4 ⇒ nKOH dư = 0,4 - 0,2 = 0,2
⇒ Chất rắn khan gồm 0,2 mol KOH, 0,16 mol CH3COOK và 0,04 mol C6H5OK
Vậy ![]()

Chọn đáp án A
nCH3COOC2H5 = 8,8/88 = 0,1 < nKOH = 0,13 Þ nKOH dư = 0,13 – 0,1 = 0,03
Phần rắn khan chứa 0,03 mol KOH và 0,1 mol CH3COOK
Vậy m = 0,03.56+0,1.98 = 11,48.

Chọn đáp án C
Ta có n C H 3 C O O C 6 H 5 = 0 , 04 và n C H 3 C O O C H 2 C 6 H 5 = 0 , 12 ,
nKOH = 0,4 mol
Ta có các phản ứng:
C H 3 C O O C 6 H 5 + 2 K O H → C H 3 C O O K + C 6 H 5 O K + H 2 O
C H 3 C O O C H 2 C 6 H 5 + K O H → C H 3 C O O K + C 6 H 5 C H 2 O H
+ Chất rắn bao gồm: KOH dư nếu có, CH3COOK và C6H5OK
⇒ m R ắ n = ( 0 , 4 – 0 , 04 × 2 – 0 , 12 ) × 56 + ( 0 , 04 + 0 , 12 ) × 98 + 0 , 04 × 132
= 32,16 gam

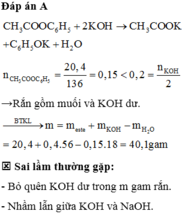
Đáp án A
nCH3COOC2H5 = 0,1 < nKOH → m = 8,8 + 0,15.56 – 0,1.46 = 12,6 gam

Đáp án A
nCH3COOC2H5 = 0,1 < nKOH → m = 8,8 + 0,15.56 – 0,1.46 = 12,6 gam

Đáp án A
Ta có phản ứng:
![]()
Ta có nEste = 0,1 mol
và nKOH = 0,15 mol > nEste
⇒ KOH dư.
+ Ta có nC2H5OH = 0,1 mol
⇒ Áp dụng định luật bảo
toàn khối lượng ta có:
mChất rắn
= 8,8 + 0,15×56 – 0,1×46
= 12,6 gam

Đáp án A
nCH3COOC2H5 = 0,1 < nKOH → m = 8,8 + 0,15.56 – 0,1.46 = 12,6 gam

Đáp án A
Ta có phản ứng:
CH3COOC2H5 + KOH → CH3COOK + C2H5OH.
Ta có
nEste = 0,1 mol và nKOH = 0,15 mol > nEste ⇒ KOH dư.
+ Ta có nC2H5OH = 0,1 mol
⇒ Áp dụng định luật bảo toàn khối lượng ta có:
mChất rắn = 8,8 + 0,15×56 – 0,1×46 = 12,6 gam