Hỗn hợp khí X gồm etilen và propin. Cho a mol X tác dụng với lượng dư dung dịch AgNO3 trong NH3 thu được 30,87 gam kết tủa. Mặt khác a mol X phản ứng tối đa với 0,56 mol H2. Giá trị của a là:
A.0,49
B.0,77
C.0,56
D.0,35
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{CAg\equiv C-CH_3}=\dfrac{30,87}{147}=0,21mol\)
\(\Rightarrow n_{propin}=0,21mol\)
Xét tỉ lệ: \(etilen:H_2=1:1\)
\(propin:H_2=1:2\)
\(\Rightarrow n_{etilen}+n_{propin}=n_{H_2}+2n_{H_2}=0,56\)
\(\Rightarrow n_{etilen}=0,56-2\cdot0,21=0,14mol\)
\(\Rightarrow a=n_{etilen}+n_{propin}=0,14+0,21=0,35mol\)

Nhận thấy đề bài cho 2 số liệu tương ứng với 2 ẩn là số mol etilen và propin, do đó một cách đơn giản và rất tự nhiên là dùng phương pháp đại số. Do đó ta thiết lập 2 phương trình 2 ẩn giải bình thường
Các phản ứng xảy ra:
![]()
![]()
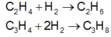
Gọi số mol của etilen và propin trong hỗn hợp lần lượt là x và y
Ta đi đến hệ
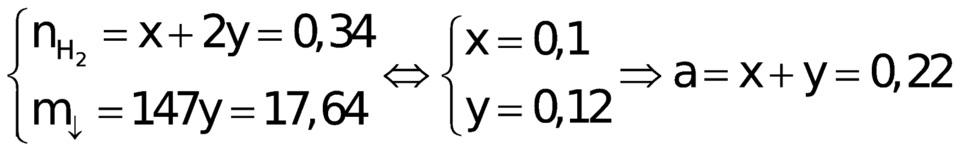
Đáp án D.

Đáp án C
Đặt số mol C2H4 = b và nC3H4 = c.
+ PT theo nH2: b + 2c = 0,44 (1).
+ PT theo khối lượng kết tủa là: 147c = 17,64 (2).
⇒ Giải hệ PT (1) và (2) ⇒ b = 0,2 và c = 0,12
⇒ nX = a = b + c = 0,32

Chọn đáp án B
HC≡C-CH3 + AgNO3 + NH3 → AgC≡C-CH3↓ + NH4NO3.
⇒ npropin = n↓ = 17,64 ÷ 147 = 0,12 mol. Lại có:
Etilen + 1H2 || Propin + 2H2 ⇒ netilen = 0,34 - 0,12 × 2 = 0,1 mol.
⇒ a = 0,1 + 0,12 = 0,22 mol ⇒ chọn B.
Đáp án D