Cho 14,2 gam P2O5 vào 200 gam dung dịch NaOH 8% thu được dung dịch A. Công thức của muối thu được và nồng độ của muối trong dung dịch A là:
A. NaH2PO4 , 11,2%
B. Na2HPO4 và 13,26%
C. Na3PO4 và 7,66%
D. Na2HPO4 và NaH2PO4 đều 7,66%
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B.
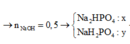
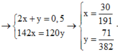
→ n P 2 O 5 = 131 764
→ B T K L m + m 17 . 32 → m = 11 , 66

nOH- = 2,4a(mol)
nH3PO4= a(mol)
=> 2< nOH-/nH3PO4= 2,4a/a=2,4<3
=> Sp thu được hỗn hợp 2 muối : Na3PO4 và Na2HPO4
=> Chọn B
Chúc em học tốt!
Đáp án B
nP2O5 =14,2 : 142 = 0,1 (mol); nNaOH = (200.8%):(100% : 40) = 0,4 (mol)
Bài toán này quy về H3PO4 tác dụng với dd NaOH
BTNT P: nH3PO4 = 2nP2O5 = 2.0,1 = 0,2 (mol)
Ta có nNaOH /nH3PO4 = 0,4 : 0,2 = 2 => Tạo muối Na2HPO4
H3PO4 + 2NaOH → Na2 HPO4 + H2O
0,2 → 0,2
mdd sau = mP2O5+ mNaOH = 14,2 + 200 = 214,2 (g)
C% Na2 HPO4 = ( mCtan/ mdd).100% = (0,2. 142 : 214,2).100% = 13,23%