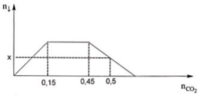
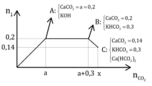
Sục CO2 vào dung dịch chứa hỗn hợp gồm Ca(OH)2 và KOH ta quan sát hiện tượng theo đồ thị hình bên (số liệu tính theo đơn vị mol). Giá trị của x là:
A. 0,12.
B. 0,11.
C. 0,13.
D. 0,10.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.





Giải thích:
Quan sát đồ thị ta thấy nCO2 = 0,15 thì kết tủa đạt max.
=> nCa(OH)2 = nCaCO3 max = 0,15
Khi nCO2 = 0,45 thì bắt đầu hòa tan kết tủa.
Khi nCO2 = 0,5 thì lượng kết tủa bị hòa tan là: nCaCO3 bị hòa tan = 0,5 - 0,45 = 0,05
=> nCaCO3 còn lại = x = 0,15 - 0,05 = 0,1
Đáp án A

Đáp án A.
Nhìn vào đồ thị ta có:
- Ứng với số mol CO2 từ 0 đến 0,15 mol có: CO2 + Ca(OH)2 CaCO3 + H2O.
số mol Ca(OH)2 = 0,15 mol và số mol kết tủa = 0,15 mol.
- Ứng với số mol CO2 từ 0,15 đến 0,45 mol có: CO2 + KOH KHCO3
- Ứng với số mol CO2 từ 0,45 đến 0,5 mol có : CO2 + CaCO3 + H2O Ca(HCO3)2.
Số mol CO2 hòa tan kết tủa = 0,05 mol lượng CaCO3 bị hòa tan = 0,05 mol còn lại 0,1 mol CaCO3.
x = 0,1 mol.

Đáp án là A
Quan sát đồ thị ta thấy số mol CO2 =0,15 thì kết tủa max
→số mol Ca(OH)2=số mol CaCO3 max=0,15 mol
Khi số mol CO2=0,45 thì bắt đầu hòa tan kết tủa
Khi số mol CO2 =0,5 thì số mol CaCO3 bị hòa tan là 0,5-0,45=0,05 mol
→số mol CaCO3 còn lại là x=0,15-0,05=0,1

Đáp án B.
Cách 1:
Tại A:
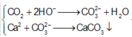
![]()
Quá trình
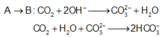
Tại C:
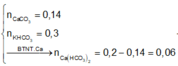
![]()
Cách 2: Phân tích đồ thị:
x = 0,2 + 0,3 + (0,2 - 0,14) = 0,56