Một bình kín có thể tích là 0,5 lit chứa 0,5 mol H2 và 0,5 molN2 , ở nhiệt độ toC . Khi ở trạng tháu cân bằng có 0,2 mol NH3 tạo thành. Hằng số cân bằng Kc của phản ứng tổng hợp NH3 là
A. 1,278
B. 3,125
C. 6,750
D. 4,125
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Theo gải thiết ban đầu ta thấy [H2]=[N2]=1M
Thực hiện phản ứng tổng hợp NH3đến thời điểm cân bằng [NH3] = 0,4 m
Ta có: N2+3H2 ⇌2NH3
Bdau: 1………1………….0
p.ung:0,2…….0,6……….0,4
Sau: 0,8………0,4……….0,4
Tại thời điểm cân bằng [N2]=0,8;[H2]=0,4M;[NH3]=0,4M →Kc = 3,125

Chọn B
Theo giả thiết ta thấy ban đầu H 2 = N 2 = 1 M .
Thực hiện phản ứng tổng hợp NH3 đến thời điểm cân bằng NH 3 = 0 , 4 M
Phương trình phản ứng hoá học :

Theo (1) tại thời điểm cân bằng [NH3] = 0,8M; [H2] =0,4M; [NH3] = 0,4M.
Vậy hằng số cân bằng của phản ứng tổng hợp NH3 là :
K C = NH 3 2 N 2 H 2 3 = ( 0 , 4 ) 2 0 , 8. ( 0 , 4 ) 3 = 3 , 125

Đáp án C.
N2+ 3H2 ⇌ 2NH3
Vì  nên hiệu suất tính theo H2
nên hiệu suất tính theo H2
N2+ 3H2 ⇌ 2NH3
Ban đầu 0,5 0,5 mol
Phản ứng x/3 x 2x/3 mol
Sau pứ 0,2 mol
Ở trạng thái cân bằng có 0,2 mol NH3 tạo thành nên 2x/3= 0,2
→x=0,3


Đáp án A
Gọi số mol N2 phản ứng là x (mol).
Phản ứng: N2 (k) + 3H2 (k) D 2NH3 (k)
Ban đầu: 0,4M 0,6M 0
Phán úng: x 3x 2x
Cần bằng: (0,4-x) (0,6-3x) 2x
H2 chiếm 25% hỗn hợp sau phản ứng nên:
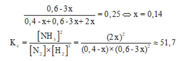

Đáp án A
Gọi số mol N2 phản ứng là x (mol).
Phản ứng: N2 (k) + 3H2 (k) D 2NH3 (k)
Ban đầu: 0,4M 0,6M 0
Phán úng: x 3x 2x
Cần bằng: (0,4-x) (0,6-3x) 2x
H2 chiếm 25% hỗn hợp sau phản ứng nên:
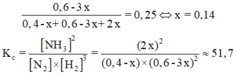
Đáp án B
Theo gải thiết ban đầu ta thấy [H2]=[N2]=1M
Thực hiện phản ứng tổng hợp NH3đến thời điểm cân bằng [NH3] = 0,4 m
Ta có: N2+3H2 ⇌2NH3
Bdau: 1………1………….0
p.ung:0,2…….0,6……….0,4
Sau: 0,8………0,4……….0,4
Tại thời điểm cân bằng [N2]=0,8;[H2]=0,4M;[NH3]=0,4M
→Kc = 3,125