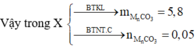
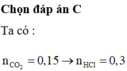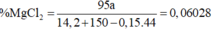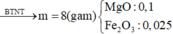Hoà tan 14,2 gam hỗn hợp X gồm MgCO3 và một muối cacbonat của kim loại M vào một lượng vừa đủ axit HCl 7,3%, thu được dung dịch Y và 3,36 lít khí CO2 (đktc). Nồng độ MgCl2 trong Y là 6,028%. Cho dung dịch NaOH dư vào dung dịch Y, lọc lấy kết tủa đem nung ngoài không khí đến khối lượng không đổi thì thu được m gam chấy rắn. Giá trị của m là
A. 7,6
B. 10,4
C. 8,0
D. 12,0