có 2 cốc khối lượng bằng nhau, mỗi cốc nặng 49g. cốc A đựng nước cất, cốc B đựng dung dịch H2SO4 loãng. cho vào mỗi cốc một cái đinh sắt nặng 2,8g, sau đó đem 2 cốc đi cân lại thì khối lượng 2 cốc có bằng nhau không? nếu khác nhau thì khác bao nhiêu gam? Mọi người giúp mình với, xin cảm ơn.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nMg=3,6/24=0,15 mol ; nAl=5,4/27=0,2 mol
1) Mg + 2HCl --> MgCl2 + H2 (1)
0,15 0,15 0,15 mol
2Al+ 3H2SO4 --> Al2(SO4)3 + 3H2 (2)
0,2 0,1 0,3 mol
b)(1) => vH2=0,15x22,4=3,36 l
(2) => V H2= 0,3x22,4=6,72 l
=> VH2(2) > VH2(1)
c) đặt dd HCl là A => dd H2SO4 = A
(1) => m dd sau = 0,15*24 + A -0,15 *2 =3,3 + A
(2) => m dd sau= 0,2*27 + A - 0,2 *2=4,8+A
=> cần thêm nước vào cốc thứ nhất và thêm số gam là
4,8 + A - (3,3 + A) = 1,5 g nước

\(n_{Fe}=\dfrac{7,84}{56}=0,14\left(mol\right);n_{Al}=\dfrac{8,1}{27}=0,3\left(mol\right)\)
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: 0,14 0,14
PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
'Mol: 0,3 0,45
⇒ Khối lượng đc thêm vào ở cốc A là 7,84-0,14.2=7,56 (g)
Khối lượng đc thêm vào ở cốc B là 8,1-0,45.2=7,2 (g)
⇒ Cốc A nặng hơn cốc B (do khối lượng axit được lấy vào 2 cốc bằng nhau )
Vậy cân ko còn ở vị trí thăng bằng

nFe =
nFe = 0.2 (mol).
nAl =
Xét thí nghiệm 1, ta có phương trình phản ứng:
Fe + 2HCl → FeCl2 + H2
0.2 0.4 0.2 0.2 (Mol)
Dung dịch sau phản ứng có chứa: FeCl2 - 0.2 mol và có thể có axit dư
Xét thí nghiệm 2, ta có phương trình phản ứng:
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
m/27 m/54 3m/54 (Mol)
Dung dịch sau phản ứng có chứa: Al2(SO4)3 hoặc có thể có axit còn dư
Vì sau khi phản ứng cái kim đồng hồ cân nặng vẫn ở vị trí cân bằng nên ta có thể suy luận như sau:
Khối lượng kim loại Nhôm khi cho vào cốc A trừ đi khối lượng đã mất đi là khí Hidro ở cốc A phải bằng Khối lượng kim loại Nhôm cho vào cốc B trừ đi lượng khí Hidro thoát ra ở cốc B
Vậy ta có phương trình cân bằng khối lượng của 2 cốc như sau:
Cốc A{mFe - mH2} = Cốc B{mAl - mH2}
11.2 - 0.2*2 = m - 6m/54
48m = 583.2
=>m = 12.15 (g)

- Cốc A: \(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\)
\(n_{CaCO_3}=\dfrac{25}{100}=0,25\left(mol\right)=n_{CO_2}\)
Có: m cốc A tăng = mCaCO3 - mCO2 = 25 - 0,25.44 = 14 (g) = m cốc B tăng
- Cốc B: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
GọI: nAl = x (mol) \(\Rightarrow n_{H_2}=\dfrac{3}{2}n_{Al}=\dfrac{3}{2}x\left(mol\right)\)
Có: m cốc B tăng = 14 (g) = 27x - 3/2x.2
⇒ x = 7/15 (mol)
\(\Rightarrow a=m_{Al}=\dfrac{7}{15}.27=12,6\left(g\right)\)

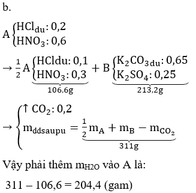
a.
|
|
AgNO3 |
K2CO3 |
| Ban đầu |
0,6 mol; 102 gam |
0,9 mol; 124,2 gam |
| Thêm vào |
→ HCl : 0 , 1 mol ↓ AgCl : 0 , 6 mol |
← H 2 SO 4 : 0 , 25 ↑ CO 2 : 0 , 25 |
| Sau phản ứng |
115,9gam |
213,2 gam |
| Thêm nước |
213,2 – 115,9 = 97,3 gam |
|

\(Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = n_{Fe} = \dfrac{11,2}{56} =0,2(mol)\\ \Rightarrow m_{tăng} = 11,2 - 0,2.2 = 10,8(gam)\\ 2Al +3 H_2SO_4 \to Al_2(SO_4)_3 + 3H_2\\ n_{Al} = \dfrac{m}{27}(mol)\\ \Rightarrow n_{H_2} = \dfrac{3}{2}n_{Al} = \dfrac{m}{18}(mol)\)
Vì cân ở vị trí thăng bằng nên :
\(m - \dfrac{m}{18}.2 = 10,8\Rightarrow m =12,15(gam)\)

\(n_{Fe}=\dfrac{11,2}{56}=0,2mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,2 0,2
\(\Rightarrow m_{Fe}+m_{H_2SO_4}=0,2\cdot56+0,2\cdot98=30,8g\)
Cả hai đĩa cân thăng bằng:
\(m_{Fe}+m_{H_2SO_4}=m_{Al}+m_{H_2SO_4}\)
\(\Rightarrow m_{Fe}=m_{Al}=11,2g\)

Bài của Minh mình thấy chưa được nha chưa trừ đi mH2 đã được giải phóng
- Xét đĩa cân có Al và H2SO4: (Gọi là đĩa A)
\(n_{Al}=\dfrac{m}{27}\left(mol\right)\)
PTHH: 2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2
\(\dfrac{m}{27}\)-->\(\dfrac{m}{18}\)--------------------------->\(\dfrac{m}{18}\)
=> mA (sau pư) = \(m+\dfrac{98m}{18}-\dfrac{2m}{18}=\dfrac{19m}{3}\left(g\right)\)
Xét đĩa cân có Mg và HCl: (Gọi là đĩa cân B)
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PTHH: Mg + 2HCl ---> MgCl2 + H2
0,2---->0,4------------------->0,2
=> mB (sau pư) = 4,8 + 0,4.36,5 - 0,2.2 = 19 (g)
Mà mA = mB
\(\rightarrow\dfrac{19m}{3}=19\\ \Leftrightarrow m=3\left(g\right)\)
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\
pthh:Mg+2HCl\rightarrow MgCl_2+H_2\)
0,2 0,4
=> \(m_{HCl}=0,4.98=39,2\left(g\right)\\
m_{Mg}+m_{HCl}=4,8+39,2=44g\)
vì 2 đĩa cân bằng nhau
=> \(m_{Mg}+m_{HCl}=m_{Al}+m_{H_2SO_4}\)
=> \(m_{Al}=m_{Mg}+m_{HCl}-m_{H_2SO_4}=4,8+39,2-39,2=4,8\left(g\right)\)
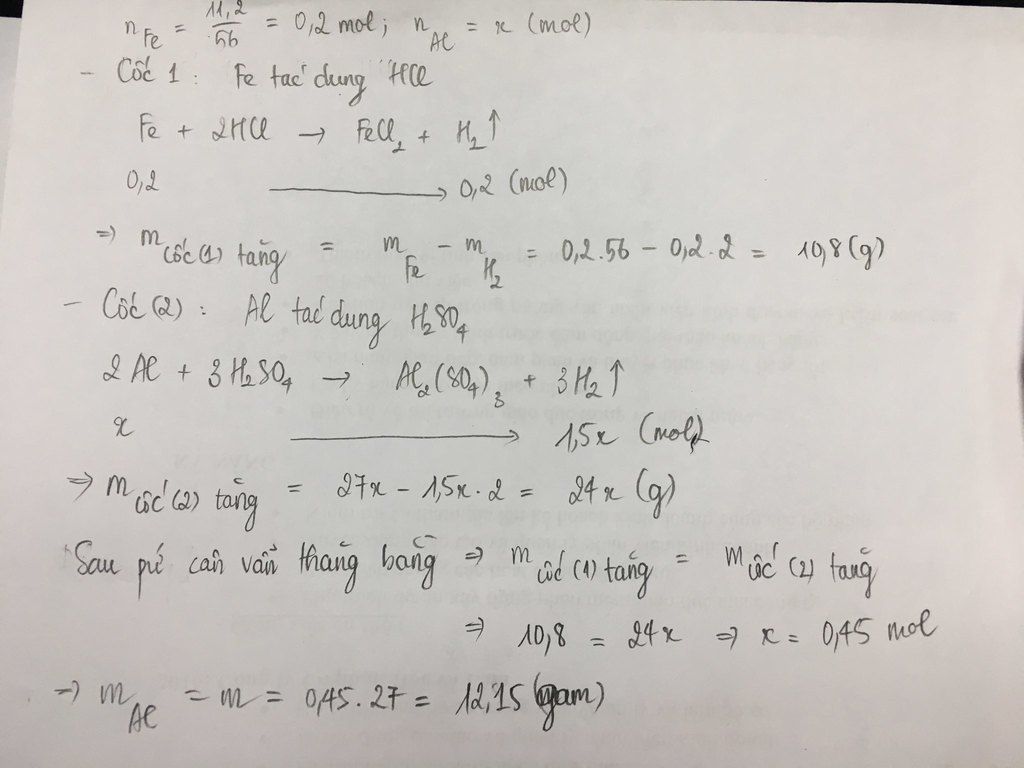
PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
Ta có: \(n_{Fe}=\dfrac{2,8}{56}=0,05\left(mol\right)=n_{H_2}\) \(\Rightarrow m_{H_2}=0,05\cdot2=0,1\left(g\right)\)
\(\Rightarrow\) Cốc B nhẹ hơn cốc A là 0,1 gam