tính thành phần phần%về khối lượng mỗi nguyên tố có trong hợp chất có CTHH: Na3PO4
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


1
\(MP_2O_3=110g/mol\)
\(\%P=\dfrac{31.2.100}{110}=58,2\%\)
\(\%O=100-58,2=41,8\%\)
2
\(MA=8.2=16g/mol\)
Tính theo hoá trị
=> cthh của A là CH\(_4\)

\(M_A=14\cdot2=28\left(g\text{/}mol\right)\)
Công thức của A là : \(C_xO_y\)
\(\%C=\dfrac{12x}{28}\cdot100\%=42.86\%\)
\(\Rightarrow x=1\)
\(M=28\left(g\text{/}mol\right)\)
\(\Rightarrow12+16y=28\)
\(\Rightarrow y=1\)
\(CT:CO\)

Câu 1:
a) Al2O3:
Phần trăm Al trong Al2O3: \(\%Al=\dfrac{27.2}{27.2+16.3}.100=52,94\%\)
Phần trăm O trong Al2O3: \(\%O=100-52,94=47,06\%\)
b) C6H12O:
Phần trăm C trong C6H12O: \(\%C=\dfrac{12.6}{12.6+12+16}.100=72\%\)
Phần trăm H trong C6H12O: \(\%H=\dfrac{1.12}{12.6+12+16}.100=12\%\)
Phần trăm O trong C6H12O : \(\%O=100-72-12=16\%\)
Câu 2:
\(m_H=\dfrac{5,88.34}{100}\approx2\left(g\right)\)
\(m_S=\dfrac{94,12.34}{100}=32\left(g\right)\)
\(n_H=\dfrac{m}{M}=\dfrac{2}{1}=2\left(mol\right)\)
\(n_S=\dfrac{m}{M}=\dfrac{32}{32}=1\left(mol\right)\)
⇒ CTHH của hợp chất: H2S

+ Bước 1: Tính M của hợp chất.
+ Bước 2: Xác định số mol nguyên tử mỗi nguyên tố trong hợp chất.
Ví dụ 1: Xác định thành phần phần trăm theo khối lượng của các nguyên tố có trong hợp chất KNO3
Lời giải
+ MKNO3 = 39_+ 14+16.3=101 gam
+ Trong 1 mol KNO3 có:
1 mol nguyên tử K
1 mol nguyên tử N
3 mol nguyên tử O
+ %K= (39.100):101=36,8%
+ %N= (14.100):101=13,8%
+ %K= (48.100):101=47,6%
Hoặc %O=100%-(36,8%+13,8%)=47,6%
Ví dụ 2: Tính thành phần phần trăm theo khối lượng của các nguyên tố có trong hợp chất Fe2O3
Lời giải
+ MFe2O3 = 56.2+16.3= 160 gam
+ Trong 1 mol Fe2O3 có:
2 mol nguyên tử Fe
3 mol nguyên tử O
+ %Fe = (112.100):160 = 70%
+ %O = (48.100):160 = 30%
Hoặc %O = 100% - 70% = 30%
*bn áp dụng theo cái này nha
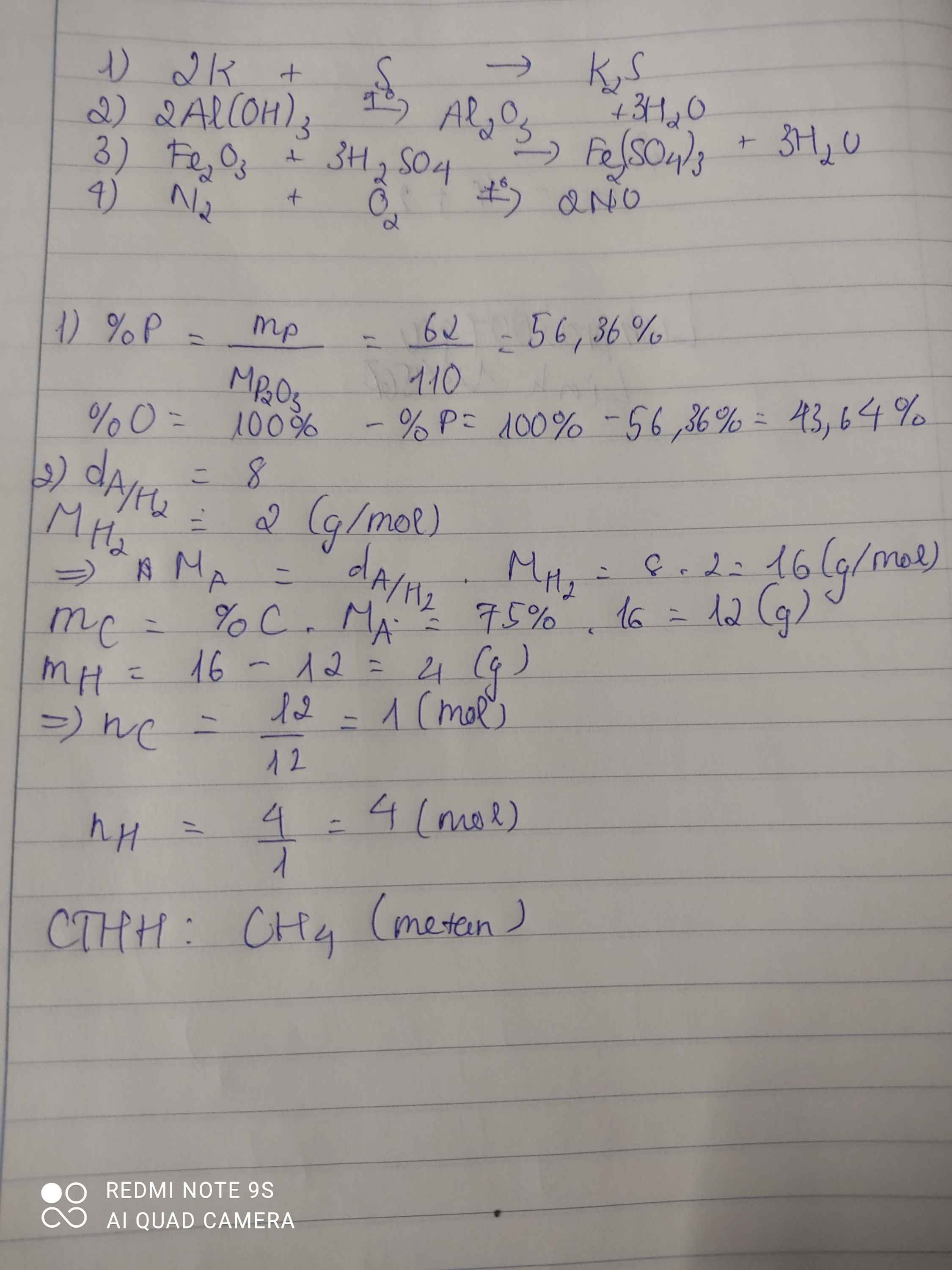
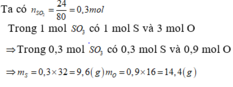

%Na = \(\dfrac{23.3}{23.3+31+16.4}\).100 =42,07%
%P = \(\dfrac{31}{23.3+31+16.4}\).100 = 18,9%
%O = 100 - 42,07 - 18,9 =39,03%