Đốt cháy hoàn toàn hợp chất hữu cơ Y cần dùng 16,8(lit) O2 thu được CO2, H2O ,N2 . Cho hoàn toàn sản phẩm thu được qua dung dịch Ca(OH)2 dư thu được 60g kết tủa đồng thời khối lượng bình giảm 21g và có 2,24(lit) khí thoát ra khỏi bình (đktc).
Tìm công thức phân tử của Y biết công thức phân tử trùng với công thức đơn giản nhất.



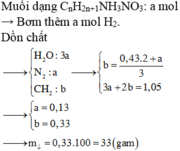
\(Đăt:n_{CO_2}=a\left(mol\right),n_{H_2O}=b\left(mol\right)\)
\(BTNTO:\\ 2n_{O_2}=2n_{CO_2}+n_{H_2O}\\ \Leftrightarrow2a+b=0.75\left(1\right)\)
\(m_{bìnhgiảm}=m_{CaCO_3}-\left(m_{CO_2}+m_{H_2O}\right)=21\left(g\right)\)
\(\Leftrightarrow44a+18b=60-21=39\left(g\right)\left(2\right)\)
Bạn xem lại đề nha
\(n_{CO_2} = n_{CaCO_3} = 0,6(mol)\)
\(m_{tăng} = n_{CO_2} + m_{H_2O} - m_{CaCO_3}\\ \Rightarrow n_{H_2O} = \dfrac{60-21-0,6.44}{18} = 0,7(mol)\)
\(n_{N_2} = n_{khí\ thoát\ ra} = 0,1(mol)\)
\(n_{O_2} =0,75(mol)\)
BTNT với C,H,O và N :
\(n_C = n_{CO_2} = 0,6\\ n_H = 2n_{H_2O} = 0,7.2 = 1,4(mol)\\ n_N = 2n_{N_2} = 0,2(mol)\\ n_O = 2n_{CO_2} + n_{H_2O} -2n_{O_2}= 0,4(mol)\)
Ta có :
\(n_C : n_H : n_O : n_N = 0,6 : 1,4 : 0,4 : 0,2 = 3 : 7 :2 : 1\)
Vậy CTPT của Y :C3H7O2N