Hòa tan hoàn toàn m gam hỗn hợp X gồm Al; Mg (tỉ lệ mol là 1:1) vào dung dịch HNO3 dư, thấy thoát ra hỗn hợp gồm 0,4 mol NO và 0,1 mol N2O
a, Xác định số mol HNO3 đã bị khử
b, Xác định số mol HNO3 đã tham gia phản ứng
c, Tính m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Do VH2 thu được ở 2 thí nghiệm khác nhau
⇒ Al dư ở thí nghiệm 1.
Đặt nNa = x; nAl = y.
● Xét thí nghiệm 1: Na → NaOH → NaAlO2.
⇒ nAl phản ứng = nNa = x.
Bảo toàn electron:
x + 3x = 2 × 0,4 ⇒ x = 0,2 mol.
● Xét thí nghiệm 2: Do NaOH dư
⇒ Al tan hết. Bảo toàn electron:
x + 3y = 2 × 0,55 ⇒ y = 0,3 mol.
||► m = 0,2 × 23 + 0,3 × 27 = 12,7(g).

Chọn đáp án D
Do VH2 thu được ở 2 thí nghiệm khác nhau ⇒ Al dư ở thí nghiệm 1.
Đặt nNa = x; nAl = y. ● Xét thí nghiệm 1: Na → NaOH → NaAlO2.
⇒ nAl phản ứng = nNa = x. Bảo toàn electron: x + 3x = 2 × 0,4 ⇒ x = 0,2 mol.
● Xét thí nghiệm 2: Do NaOH dư ⇒ Al tan hết. Bảo toàn electron:
x + 3y = 2 × 0,55 ⇒ y = 0,3 mol. ||► m = 0,2 × 23 + 0,3 × 27 = 12,7(g)

Đáp án C
Khi cho X vào H2O thì thu được 0,4 mol H2 còn khi cho vào NaOH thì thu được 0,55 mol H2 chứng tỏ khi cho vào H2O thì NaOH dư.
Gọi số mol Na và Al lần lượt là a, b
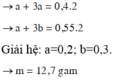

Đáp án D
Nhận thấy khi cho vào nước lượng H2 nhỏ hơn khi cho vào NaOH. Do vậy khi cho X vào nước thì Al dư.
Gọi số mol Na là x, Al là y.
Khi cho X vào nước, Al dư nên số mol Al phản ứng bằng số mol Na x+x.3 = 0,4.2
Cho X vào NaOH thì cả 2 phản ứng hết → x+3y=0,55.2
Giải được: x = 0,2; y = 0,3 → m = 12,7 gam

Đáp án D
nH2(1) = 8,96 : 22,4 = 0,4 (mol)
nH2(2) = 12,32 : 22,4 = 0,55 (mol)
Gọi mol nNa = x (mol); nAl = y (mol)
Bảo toàn e: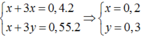
m = 0,2.23 + 0,3. 27 = 12,7(gam)

Giải thích:
nH2(1) = 8,96 : 22,4 = 0,4 (mol)
nH2(2) = 12,32 : 22,4 = 0,55 (mol)
Gọi mol nNa = x (mol); nAl = y (mol)
Bảo toàn e:
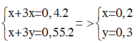
m = 0,2.23 + 0,3. 27 = 12,7(gam)
Đáp án D

Đáp án D
nH2(1) = 8,96 : 22,4 = 0,4 (mol)
nH2(2) = 12,32 : 22,4 = 0,55 (mol)
Gọi mol nNa = x (mol); nAl = y (mol)
Bảo toàn e:
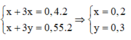
m = 0,2.23 + 0,3. 27 = 12,7(gam)

Có mrắn tăng=m+12,8-m=12,8\(\Rightarrow\)\(m_O=12,8\Rightarrow n_{O^{2-}}=n_O=0,4mol\)
\(2H^+\) + \(O^{2-}\) \(\rightarrow\) \(H_2O\)
0,8 \(\leftarrow\) 0,4
\(n_{HNO_3}=n_{H^+}=0,8mol\)\(\Rightarrow V_{HNO_3}=\dfrac{0,8}{2}=0,4l=400ml\)
a, BTNT N, có: nHNO3 (bị khử) = nNO + 2NN2O = 0,4 + 2.0,1 = 0,6 (mol)
b, Giả sử: nAl = mMg = x (mol)
Các quá trình:
\(Al^0\rightarrow Al^{+3}+3e\)
x___________ 3x (mol)
\(Mg^0\rightarrow Mg^{+2}+2e\)
x_____________ 2x (mol)
\(N^{+5}+3e\rightarrow N^{+2}\)
_____ 1,2 __ 0,4 (mol)
\(2N^{+5}+8e\rightarrow N_2^{+1}\)
_______0,8__0,1 (mol)
Theo ĐLBT mol e, có: 3x + 2x = 1,2 + 0,8 ⇒ x = 0,4 (mol)
⇒ nAl = nMg = 0,4 (mol)
BTNT Al, có: nAl(NO3)3 = nAl = 0,4 (mol)
BTNT Mg, có: nMg(NO3)2 = nMg = 0,4 (mol)
BTNT N, có: nHNO3 (pư) = 3nAl(NO3)3 + 2nMg(NO3)2 + nNO + 2nN2O
= 3.0,4 + 2.0,4 + 0,4 + 2.0,1 = 2,6 (mol)
c, m = mAl + mMg = 0,4.27 + 0,4.24 = 20,4 (g)
Bạn tham khảo nhé!