tính khối lượng khí oxi cần dùng để đốt cháy hoàn toàn 1kg than (chứa 84% cacbon ) biết những hợp chất còn lại không cháy được
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Khối lượng C chứa trong 1 tấn than:
PTHH: \(C+O_2\xrightarrow[]{t^o}CO_2\)
12---32-------gam
0,96--x-------tấn
\(\Rightarrow x=\dfrac{0,96.32}{12}=2,56\left(\text{tấn}\right)\)

Khối lượng C có trong 1,5 tấn than là: \(m_C=\dfrac{1,5.95}{100}=1,425\) (g)
\(n_C=\dfrac{m}{M}=\dfrac{1,425}{12}=\dfrac{19}{160}\)(mol)
PTHH: C + O2 → CO2
Theo PT: \(n_{O_2}=n_C=\dfrac{19}{160}\)
Khối lượng khí oxi cần dùng là: \(m_{O_2}=n.M=\dfrac{19}{160}.32=3,8\)(g)

Ta có: \(m_C=1,5.1000.90\%=1350\left(g\right)\)
\(n_C=\dfrac{1350}{12}=112,5\left(mol\right)\)
PT: \(C+O_2\underrightarrow{t^o}CO_2\)
Theo PT: \(n_{O_2}=n_C=112,5\left(mol\right)\)
\(\Rightarrow V_{O_2}=112,5.22,4=2520\left(l\right)\)
\(V_{kk}=V_{O_2}.5=12600\left(l\right)\)

a) Ta có PTHH
C + O2 \(\rightarrow\) CO2
mC(phản ứng) = 1 . 95% = 0.95 (tấn)
theo PT: 32g O2 : 12g C
theo ĐB : x tấn O2 : 0.95 tấn C
=> x = 0.95 x 32 : 12 =2.533 (tấn)
vậy mO2 = 2.533 tấn
b) ta có PTHH
CH4 + 2O2 \(\rightarrow\) 2H2O + CO2
Theo PT : 16g CH4 : 64g O2
Theo ĐB : 4kg CH4 : x kg O2
=> x = 4 x 64 : 16 =16 kg O2
c) Ta cóPTHH
2H2 + O2 \(\rightarrow\) 2H2O (1)
CH4 + 2O2 \(\rightarrow\) CO2 + 2H2O (2)
CÓ:
nH2 = m/M = 8/2 = 4 (mol)
nCH4 = m/M = 2/16 =0.125(mol)
theo PT(1)=> nO2 = 1/2 . nH2 = 1/2 . 4 =2 (mol)
theo PT(2) => nO2 =2 . nCH4 = 2 x 0.125 =0.25(mol)
=> tổng nO2 = 2 + 0.25 = 2.25(mol)
=> mO2 = n . M = 2.25 x 32 =72(g)

1)
mC = 5000*0.9 = 4500 (g)
nC = 4500/12 = 375 (mol)
C + O2 -to-> CO2
375__375
Vkk = 5VO2 = 375*22.4*5 = 42000(l)
2)
nP = 6.2/31 = 0.2 (mol)
nO2 = 8.96/22.4 = 0.4 (mol)
4P + 5O2 -to-> 2P2O5
0.2___0.25_____0.1
mP2O5 = 0.1*142=14.2 (g)

nKNO3 = 0.2 (mol)
2KNO3 -to-> 2KNO2 + O2
0.2__________0.2____0.1
mKNO2 = 0.2*85=17(g)
C + O2 -to-> CO2
x___x
S + O2 -to-> SO2
y___y
x + y = 0.1 (1)
Mặt khác :
+) 32y/m * 100% = 4%
=> 32y = 0.04m (2)
+) 12x/m = 0.92
=> 12x = 0.92m (3)
(1) , (2) , (3) :
x = 0.1
y = 0.002
m = 1.3
VCO2 + VSO2 = ( 0.1 + 0.002) * 22.4 = 2.2848 (l)
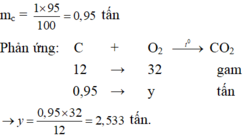
\(m_C=84\%.1000=840\left(g\right)\Rightarrow n_C=\dfrac{840}{12}=70\left(mol\right)\\ C+O_2\rightarrow\left(t^o\right)CO_2\\ n_{O_2}=n_C=70\left(mol\right)\Rightarrow m_{O_2}=70.32=2240\left(g\right)\)