Dẫn từ từ 4,48 lít hỗn hợp khí etilen và propilen (đktc) vào dung dịch brom dư thấy khối lượng bình brom tăng 7,7 gam. Tính % thể tích của mỗi khí trong hỗn hợp ban đầu.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{C_2H_4} = a\ mol;n_{C_3H_6} = b\ mol\\ \Rightarrow a + b = \dfrac{3,36}{22,4} = 0,15(1)\\ C_2H_4 + Br_2 \to C_2H_4Br_2\\ C_3H_6 + Br_2 \to C_3H_6Br_2\\ m_{tăng} = 28a + 42b = 4,9(2)\\ (1)(2)\Rightarrow a = 0,1; b = 0,05\\ \%V_{C_2H_4} = \dfrac{0,1}{0,15}.100\% = 66,67\%\\ \%V_{C_3H_6} = 100\% -66,67\% = 33,33\%\)

Gọi số mol của etilen và propilen lần lượt là x và y mol.
Khối lượng dung dịch sau phản ứng tăng lên chính là khối lượng của hỗn hợp etilen và propilen.
Ta có hệ phương trình:
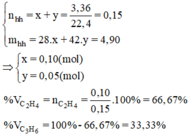

\(m_{tăng}=m_{C_2H_2}=1,3\left(g\right)\\ \Rightarrow n_{C_2H_2}=\dfrac{1,3}{26}=0,05\left(mol\right)\\ \Rightarrow\%V_{\dfrac{C_2H_2}{A}}=\dfrac{0,05.22,4}{4,48}.100=25\%\\ \Rightarrow\%V_{\dfrac{CH_4}{A}}=100\%-25\%=75\%\)

\(n_{hhkhí\left(C_2H_4,CH_4\right)}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
\(m_{tăng}=m_{C_2H_4}=4,2\left(g\right)\\ n_{C_2H_4}=\dfrac{4,2}{28}=0,15\left(mol\right)\\ \%V_{C_2H_4}=\dfrac{0,15}{0,35}=42,85\%\\ \%V_{CH_4}=100\%-42,85\%=57,15\%\)
\(Đặt:n_{C_2H_4}=a\left(mol\right);n_{C_3H_6}=b\left(mol\right)\left(a,b>0\right)\\ C_2H_4+Br_2\rightarrow C_2H_4Br_2\\ C_3H_6+Br_2\rightarrow C_3H_6Br_2\\ m_{tăng}=m_{hh.ban.đầu}=7,7\left(g\right)\\ \Rightarrow Hpt:\left\{{}\begin{matrix}28a+42b=7,7\\a+b=0,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,05\\b=0,15\end{matrix}\right.\)
Vì thể tích tỉ lệ thuận với số mol nên ta có:
\(\%V_{C_2H_4\left(đktc\right)}=\%n_{C_2H_4}=\dfrac{a}{a+b}.100\%=\dfrac{0,05}{0,2}.100=25\%\\ \Rightarrow\%V_{C_3H_6}=100\%-25\%=75\%\)