cho hỗn hợp giòm 2 hữu cơ có CTPT CnH2n+2, CmH2m. đốt 11,2(l) hỗn hợp khí A được 33,6(l) CO2 đktc và 30,6(g) H2O. xác định %V hỗn hợp
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


$n_{CO_2} = 0,7(mol) ; n_{H_2O} = 0,8(mol)$
$n_A = n_{H_2O} - n_{CO_2} = 0,8 - 0,7 = 0,1(mol)$
$n_B = \dfrac{6,72}{22,4} - 0,1 = 0,2(mol)$
Bảo toàn nguyên tố với C :
$n_{CO_2} = 0,1n + 0,2m = 0,7$
Với n = 3 ; m = 2 thỉ thỏa mãn
Với n = 1 ; m = 3 thì thỏa mãn
Vạy A và B có thể là $C_3H_8,C_2H_4$ hoặc $CH_4,C_3H_6$

nCO2 = 2,688/22,4 = 0,12 mol; nH2O = 2,52/18 = 0,14 mol
Ta thấy nH2O>nCO2 => ancol là ancol no, đơn chức, mạch hở
Gọi công thức chung của ancol là CkH2k+2O (k €N*)
Giả sử:
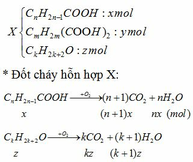
=> nH2O – nCO2 = nx – (n+1)x + (m+1)y – (m+2)y + (k+1)z – kz
=> 0,14 – 0,12 = -x - y + z hay -x - y + z = 0,02 (1)
BTNT ta tính được số mol của các nguyên tố:
nC = nCO2 = 0,12 mol
nH = 2nH2O = 2.0,14 = 0,28 mol
nO = 2nCnH2n-1COOH + 4nCmH2m(COOH)2 + nCkH2k+2O = 2x + 4y + z
=> mX = mC + mH + mO = 0,12.12 + 0,28.1 + 16(2x + 4y + z) = 32x + 64y + 16z + 1,72
* Phản ứng este hóa: Do sau phản ứng chỉ thu được chất có chứa chức este nên axit và ancol phản ứng vừa đủ
n ancol = x + 2y = z hay x + 2y – z = 0 (2)
BTKL ta có: mX = m este + mH2O => 32x + 64y + 16z + 1,72 = 3,22 + 18(x+2y)
hay 14x + 28y + 16z = 1,5 (3)
Từ (1) (2) (3) ta có hệ phương trình:
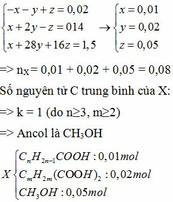
Bảo toàn nguyên tố C ta có: 0,01n + 0,02m + 0,05.1 = 0,12
=> n +2m = 7 mà do n≥3, m≥2 nên chỉ có cặp n = 3, m = 2 thỏa mãn
Vậy các axit trong X là: CH2=CH-COOH và HOOC-COOH.
Kết luận: Hỗn hợp X gồm các chất CH2=CH-COOH, HOOC-COOH và CH3OH.
- Một số ứng dụng của PVC trong thực tế như làm ống dẫn nước, vỏ dây điện, đồ giả da, áo mưa, nhãn chai nước khoáng, …

n O 2 = 11,2/32 = 0,35 mol
n C O 2 = 8,8/44 = 0,2 mol ⇒ n C = 0,2 mol
n H 2 O = 5,4/18 = 0,3 mol
⇒ n H = 2.0,3 = 0,6 mol
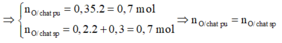
Vậy hợp chất hữu cơ A chỉ có C và H.
Gọi CTTQ của A là C x H y , khi đó ta có:
Vậy CTĐGN của A là C H 3 n
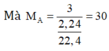
⇒ n = 30/15 = 2
Vậy A là C 2 H 6 .
⇒ Chọn A.

a, \(CH_4+2O_2\underrightarrow{t^o}CO_2+H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Ta có: \(n_{CH_4}+n_{C_2H_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\left(1\right)\)
Theo PT: \(n_{CO_2}=n_{CH_4}+2n_{C_2H_2}=\dfrac{56}{22,4}=2,5\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,5\left(mol\right)\\n_{C_2H_2}=1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,5.22,4}{33,6}.100\%\approx33,33\%\\\%V_{C_2H_2}\approx66,67\%\end{matrix}\right.\)
b, Theo PT: \(n_{O_2}=2n_{CH_4}+\dfrac{5}{2}n_{C_2H_2}=3,5\left(mol\right)\Rightarrow m_{O_2}=3,5.32=112\left(g\right)\)

Gọi 3a là số mol CO2 \(\rightarrow\)nH2O=2a mol
BTKL ta có
44.3a+18.2a=18+16,8/22,4.32
\(\rightarrow\)a=0,25 mol
\(\rightarrow\)nCO2=0,75 mol nH2O=0,5 mol
\(\rightarrow\)nC=0,75 mol nH=1 mol
Ta có 0,75.12+1=10<18 \(\rightarrow\) Trong A có O
mO trong A=18-10=8 g
nO=\(\frac{8}{16}\)=0,5 mol
Gọi CTHH là CxHyOz
Ta có x: y: z=nC: nH : nO=0,75 : 1 : 0,5 =3:4:2
\(\rightarrow\)CT đơn giản nhất là C3H4O2
mà MA=36x2=72
\(\rightarrow\)72n=72\(\rightarrow\)n=1
Vậy CTPT của A là C3H4O2

a, b là số mol X và Y
\(n_{O_2}=0,55mol;n_{CO_2}=0,35\)
\(C_nH_{2n+2}+\left(\dfrac{3n+1}{2}\right)O_2\rightarrow nCO_2+\left(n+1\right)H_2O\)
a--------------\(\dfrac{3n+1}{2}a\) ------------\(na\)
\(C_mH_{2m-2}+\left(\dfrac{3m-1}{2}\right)O_2\rightarrow mCO_2+\left(m-1\right)H_2O\)
b---------------\(\dfrac{3m-1}{2}b\)------------\(mb\)
Ta có:
\(\left\{\begin{matrix}a+b=0,25\\\dfrac{3n+1}{2}a+\dfrac{3m-1}{2}b=0,55\\na+mb=0,35\end{matrix}\right.\)\(\Leftrightarrow\left\{\begin{matrix}a+b=0,25\\a-b=0,05\\na+mb=0,35\end{matrix}\right.\)\(\Leftrightarrow\left\{\begin{matrix}a=0,15\\b=0,1\\3n+2m=7\end{matrix}\right.\)
\(\Rightarrow n=1;m=2\)\(\Rightarrow X:CH_4;Y:C_2H_2\)

Khi cho hỗn hợp A qua dung dịch brom dư, có phản ứng :
C 2 H 2 + 2 Br 2 → C 2 H 2 Br 4
Vì phản ứng xảy ra hoàn toàn và có hai khí thoát ra khỏi dung dịch brom, nên hai khí đó là CH 4 và C n H 2 n + 2
Theo đề bài V C 2 H 2 tham gia phản ứng là : 0,896 - 0,448 = 0,448 (lít).
Vậy số mol C 2 H 2 là 0,448/22,4 = 0,02 mol
Gọi số mol của CH 4 là X. Theo bài => số mol của C n H 2 n + 2 cũng là x.
Vậy ta có : x + x = 0,448/22,4 = 0,02 => x = 0,01
Phương trình hoá học của phản ứng đốt cháy hỗn hợp :
2 C 2 H 2 + 5 O 2 → 4 CO 2 + 2 H 2 O
CH 4 + 2 O 2 → CO 2 + 2 H 2 O
2 C n H 2 n + 2 + (3n+1) O 2 → 2n CO 2 + 2(n+1) H 2 O
Vậy ta có : n CO 2 = 0,04 + 0,01 + 0,01n = 3,08/44 => n = 2
Công thức phân tử của hiđrocacbon X là C 2 H 6
Gọi \(\left\{{}\begin{matrix}n_{C_nH_{2n+2}}=a\left(mol\right)\\n_{C_mH_{2m}}=b\left(mol\right)\end{matrix}\right.\)
=> \(a+b=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(n_{CO_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\)
\(n_{H_2O}=\dfrac{30,6}{18}=1,7\left(mol\right)\)
Bảo toàn C: an + bm = 1,5
=> 2an + 2bm = 3 (1)
Bảo toàn H: 2an + 2a + 2bm = 3,4 (2)
(2) - (1) => 2a = 0,4
=> a = 0,2 (mol)
\(\%V_{C_nH_{2n+2}}=\dfrac{0,2}{0,5}.100\%=40\%\)
\(\%V_{C_mH_{2m}}=100\%-40\%=60\%\)