Tính chất vật lý, tính chất hóa học của oxi? (mỗi tính chất minh họa băng 1 PTHH)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


- Tác dụng với kim loại: O2 oxi hóa được hầu hết các kim loại trừ Ag, Au, Pt.
Cu + O2 \(\Rightarrow t^o\)\(2CuO\)\(\)
- Tác dụng với hiđro, phản ứng có thể gây nổ mạnh nếu tỉ lệ thể tích O2 : H2 = 1:2
2H2 + O2 \(2H_2O\)
- Tác dụng với một số phi kim khác:
4P + 5O2 \(\rightarrow t^o\)\(2P_2O_5\)
+ Tác dụng với một số hợp chất:
2C2H6 + 7O2 \(\rightarrow t^o4CO_2\)\(+6H_2O\)

REFER
Khí oxi là một đơn chất phi kim rất hoạt động, đặc biệt ở nhiệt độ cao, dễ dàng tham gia phản ứng hóa học với nhiều phi kim, nhiều kim loại và hợp chất. Trong các hợp chất hóa học, nguyên tố oxi có hóa trị II.
Cụ thể:
- Tác dụng với kim loại: O2 oxi hóa được hầu hết các kim loại trừ Ag, Au, Pt.
Ví dụ:
- Tác dụng với hiđro, phản ứng có thể gây nổ mạnh nếu tỉ lệ thể tích O2 : H2 = 1:2
Phương trình hóa học:
- Tác dụng với một số phi kim khác:
Ví dụ:
+ Tác dụng với một số hợp chất:
Ví dụ:

- Tác dụng với kim loại:
Nước có thể tác dụng với một số kim loại ở nhiệt độ thường như Ca, Ba, K,…
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
\(K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\)
- Tác dụng với một số oxit bazo như CaO, K2O,… tạo ra bazo tương ứng Ca(OH)2, KOH,…
\(K_2O+H_2O\rightarrow2KOH\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
- Tác dụng với oxit axit như SO3, P2O5… tạo thành axit tương ứng H2SO4, H3PO4,…
\(SO_3+H_2O\rightarrow H_2SO_4\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)

Câu 1 tính chất vật lý : ko màu ko mù vị , ít tan trong nước , nặng hơn kk
. hóa lỏng ở -183oC có màu xanh nhạt
tính chất hóa học : rất hoát động ở nhiệt độ cao . có thể tác dụng với phi kim , kim loại và hợp chất
VD :td với phi kim S+O2 -t--> SO2
VD :td với kim loại 3Fe+ 2O2 -t---> Fe3O4
bài 2 :
- thu khí O2 ở bằng cách đun nóng nhuengx hợp chất giàu O2 và dễ bị phân hủy như KMnO4 . KClO3
pthh : 2KMnO4 --t--> K2MnO4 + MnO2 + O2
- thu khí oxi bằng cách đẩy kk và đẩy nước
bài 3
dạng tổng quát : M2Ox ( M là đơn chất )
- cách gọi tên : tên nguyên tố +oxit

Phản ứng của kim loại với phi kim:
- Tác dụng với oxi: \(2Cu+O_2\rightarrow2CuO\)
- Tác dụng với phi kim khác: \(4Fe+3O_2\rightarrow2Fe_2O_3\)
Phản ứng của kim loại với dd axit: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Phản ứng của kim loại với dd muối: \(Zn+CuSO_4\rightarrow ZnSO_4+CU\)

Tính chất hóa học :
- Tác dụng với kim loại tạo oxit bazo hoặc oxit lưỡng tính
$4Na + O_2 \xrightarrow{t^o} 2Na_2O$
$3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4$
- Tác dụng với phi kim tạo oxit trung tính, oxit axit,..
$S + O_2 \xrightarrow{t^o} SO_2$
$2C + O_2 \xrightarrow{t^o} 2CO$
- Tác dụng với một số hợp chất khác :
$2CO + O_2 \xrightarrow{t^o} 2CO_2$
$CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O$
$4FeS_2 + 11O_2 \xrightarrow{t^o} 2Fe_2O_3 + 8SO_2$
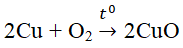
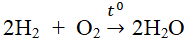
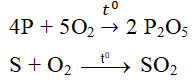
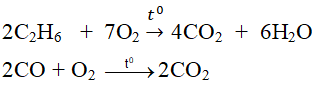

- Tác dụng được với nhiều phi kim (trừ Cl2, Br2, I2, F2,...)
\(Si+O_2\underrightarrow{t^o}SiO_2\\ 4P+5O_2\underrightarrow{t^o}2P_2O_5\)
- Tác dụng được với nhiều kim loại (trừ Ag, Pt, Au,...)
\(2Mn+O_2\underrightarrow{t^o}2MnO\\ 4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
- Tác dụng được với nhiều hợp chất:
\(4FeS_2+11O_2\underrightarrow{t^o}2Fe_2O_3+8SO_2\uparrow\\ 2SO_2+O_2\xrightarrow[V_2O_5]{t^o}2SO_3\)