Câu 6. Đốt cháy hoàn toàn 6,2g photpho trong không khí.
a.Tính thể tích không khí cần dùng ở đktc. Biết thể tích Oxi chiếm 1/5 thể tích không khí.
b. Tính khối lượng kali pemanganat cần dùng để điều chế lượng oxi nói trên.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

4P (0,2 mol) + 5O2 (0,25 mol) \(\underrightarrow{t^o}\) 2P2O5.
a) Thể tích không khí cần dùng ở đktc là 0,25.22,4.5=28 (lít).
b) 2KMnO4 (0,5 mol) \(\underrightarrow{t^o}\) K2MnO4 + MnO2 + O2 (0,25 mol).
Khối lượng cần tìm là 0,5.158=79 (g).
a.\(n_P=\dfrac{6,2}{31}=0,2mol\)
\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
0,2 0,25 ( mol )
\(V_{kk}=V_{O_2}.5=\left(0,25.22,4\right).5=28l\)
b.\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,5 0,25 ( mol )
\(m_{KMnO_4}=0,5.158=79g\)

a)
\(4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\)
Sản phẩm : Điphotpho pentaoxit.
b)
\(n_P = \dfrac{6,2}{31} = 0,2(mol)\\ \Rightarrow n_{P_2O_5} = \dfrac{1}{2}n_P = 0,1(mol)\\ \Rightarrow m_{P_2O_5} = 0,1.142 = 14,2(gam)\)
c)
\(n_{O_2} = \dfrac{5}{4}n_P = 0,125(mol)\\ \Rightarrow V_{O_2} = 0,125.22,4 = 2,8(lít)\)
d)
\(V_{không\ khí} = \dfrac{2,8}{20\%} = 14(lít)\)

a.b.
\(n_{Fe}=\dfrac{16,8}{56}=0,3mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,3 0,2 0,1 ( mol )
\(m_{Fe_3O_4}=0,1.232=23,2g\)
\(V_{O_2}=0,2.22,4=4,48l\)
\(V_{kk}=4,48.5=22,4l\)
c.
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,4 0,2 ( mol )
\(m_{KMnO_4}=\dfrac{0,4.158}{\left(100-20\right)\%}=79g\)
a/ Số mol Fe là : nFe = 16,8: 56 = 0,3 mol
PTPƯ:
3Fe + 2O2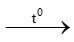 Fe3O4 (1)
Fe3O4 (1)
0,3 mol → 0,2mol → 0,1 mol
Từ (1) ta có số mol Fe3O4 = 0,1mol
→ m Fe3O4 = n.M = 0,1.232 = 23,2gam
b/ Từ (1) ta có số mol O2 đã dùng nO2 = 0,2 mol
Thể tích khí oxi đã dùng ở đktc: VO2 = n.22,4 = 0,2.22,4 = 4,48 lít
Thể tích không khí đã dùng: Vkk = 5. VO2= 5.4,48 = 22,4 lít.
c/ PTPƯ
2 KMnO4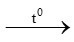 K2MnO4 + MnO2 + O2 (2)
K2MnO4 + MnO2 + O2 (2)
0,4444mol ← 0,222mol
Vì lượng Oxi thu được hao hụt 10% nên số mol O2 cần có là:
nO2 = 0,2mol.100/90 = 0.222 mol
Từ (2) ta có số mol KMnO4 = 0,444mol
Khối lượng KMnO4 bị nhiệt phân
mKMnO4 = n.M = 0,444.158 = 70.152 gam

a, \(2Zn+O_2\underrightarrow{t^o}2ZnO\)
b, \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{Zn}=0,1\left(mol\right)\Rightarrow V_{O_2}=0,1.22,4=2,24\left(l\right)\)
\(\Rightarrow V_{kk}=5V_{O_2}=11,2\left(l\right)\)
c, \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
Theo PT: \(n_{KMnO_4}=2n_{O_2}=0,2\left(mol\right)\Rightarrow m_{KMnO_4}=0,2.158=31,6\left(g\right)\)

Theo gt ta có: $n_{H_2}=0,75(mol)$
a, $2H_2+O_2\rightarrow 2H_2O$
Ta có: $n_{O_2}=0,5.n_{H_2}=0,375(mol)\Rightarrow V_{O_2}=8,4(l)\Rightarrow V_{kk}=42(l)$
b, $2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2$
Ta có: $n_{KMnO_4}=2.n_{O_2}=0,75(mol)\Rightarrow m_{KMnO_4}=118,5(g)$
a)
\(2H_2 + O_2 \xrightarrow{t^o} 2H_2O\\ V_{O_2} = \dfrac{V_{H_2}}{2} = \dfrac{16,8}{2} = 8,4(lít)\\ V_{không\ khí} = \dfrac{8,4}{20\%} = 42(lít)\)
b)
\(n_{O_2} = \dfrac{8,4}{22,4} = 0,375(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ n_{KMnO_4} = 2n_{O_2} = 0,75(mol)\\ \Rightarrow m_{KMnO_4} = 0,75.158 = 118,5(gam)\\ 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ n_{KClO_3} = \dfrac{2}{3}n_{O_2} = 0,25(mol)\\ \Rightarrow m_{KClO_3} = 0,25.122,5 = 30,625(gam)\)

\(n_{P_2O_5}=\dfrac{21,3}{142}=0,15\left(mol\right)\)
PTHH: 4P + 5O2 --to--> 2P2O5
0,3 0,375 0,15
\(\rightarrow\left\{{}\begin{matrix}m_P=0,3.31=9,3\left(g\right)\\V_{O_2}=0,375.22,4=8,4\left(l\right)\\V_{kk}=8,4.5=42\left(l\right)\end{matrix}\right.\)
PTHH: 2KClO3 --to--> 2KCl + 3O2
0,25 0,375
=> mKClO3 = 0,25.122,5 = 30,625 (g)
\(nP_2O_5=\dfrac{21,3}{142}=0,15\left(mol\right)\)
\(pthh:4P+5O_2-t^o->2P_2O_5\)
0,3 0,375 0,15
=> \(m_P=0,3.31=9,3\left(g\right)\)
=>\(V_{O_2}=0,375.22,4=8,4\left(L\right)=>V_{KK}=8,4:20\%=42\left(L\right)\)
\(pthh:2KMnO_4-t^o->K_2MnO_4+MnO_2+O_2\)
0,75 0,75
=> mKMnO4 = 0,75 . 158 = 118,5 (G)

a) nFe = 16,8/56 = 0,3 (mol)
PTHH: 3Fe + 2O2 -> (t°) Fe3O4
Mol: 0,3 ---> 0,2 ---> 0,1
mFe3O4 = 0,1 . 232 = 23,2 (g)
b) VO2 = 0,2 . 22,4 = 4,48 (l)
Vkk = 4,48 . 5 = 22,4 (l)
c) H = 100% - 20% = 80%
nO2 (LT) = 0,2 : 80% = 0,25 (mol)
PTHH: 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
nKMnO4 = 0,25 . 2 = 0,5 (mol)
mKMnO4 = 0,5 . 158 = 79 (g)

nAl = 10,8: 27=0,4 (mol)
pthh : 4Al + 3O2 -t--->2 Al2O3
0,4---> 0,3 (mol)
=>VO2 = 0,3 .22,4 = 6,72 (l)
ta có : VO2 = 1/5 Vkk <=> Vkk = VO2 : 1/5= 33,6 (l)
pthh : 2KClO3 -t--> 2KCl + 3O2
0,2<---------------------0,3 (mol)
=> mKClO3 = 0,2 . 122,5 (g)
pthh : 2KMnO4-t--> K2MnO4 + MnO2+ O2
0,6<-------------------------------- 0,3(mol)
=> mKMnO4 = 0,6.158 = 94,8 (g)
a) \(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\)
PTHH: 4P + 5O2 --to--> 2P2O5
0,2-->0,25
=> VO2 = 0,25.22,4 = 5,6 (l)
=> Vkk = 5,6.5 = 28 (l)
b)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,5<-----------------------------0,25
=> \(m_{KMnO_4}=0,5.158=79\left(g\right)\)