Đốt cháy hoàn toàn 17,4 gam hỗn hợp X gồm Al và Mg cần dùng 12,8 gam khí oxi thu được hỗn hợp oxit Y. Tính khối lượng hỗn hợp Y thu được?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Phản ứng xảy ra:
\(2Mg+O_2\rightarrow^{t^o}=2MgO\)
\(4Al+3O_2\rightarrow^{t^o}2Al_2O_3\)
Gọi số mol của Mg là x; số mol của Al là y
\(\rightarrow m_{hh}=m_{Mg}+m_{Al}=24x+2yy=17,4g\)
Có:
\(n_{MgO}=n_{Mg}=x\)
\(n_{Al_2O_3}=\frac{1}{2}n_{Al}=0,5y\)
\(\rightarrow m_Y=40x+102.0,5y=30,2g\)
\(\rightarrow\hept{\begin{cases}x=0,5\\y=0,2\end{cases}}\)
\(\rightarrow n_{MgO}=n_{Mg}=0,5mol\)
\(\rightarrow m_{MgO}=0,5.40=20g\)

PTHH: \(2Mg+O_2\underrightarrow{t^o}2MgO\) (1)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\) (2)
a) Gọi số mol của Mg là a (mol) \(\Rightarrow n_{Al}=\dfrac{2}{3}a\left(mol\right)\)
\(\Rightarrow24a+27\cdot\dfrac{2}{3}a=6,3\) \(\Rightarrow a=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{MgO}=0,15\left(mol\right)\\n_{Al_2O_3}=0,05\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{MgO}=0,15\cdot40=6\left(g\right)\\m_{Al_2O_3}=0,05\cdot102=5,1\left(g\right)\end{matrix}\right.\)
b) Theo các PTHH: \(\left\{{}\begin{matrix}n_{O_2\left(1\right)}=0,075\left(mol\right)\\n_{O_2\left(2\right)}=0,075\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\Sigma n_{O_2}=0,15\left(mol\right)\) \(\Rightarrow V_{O_2}=0,15\cdot22,4=3,36\left(l\right)\)

Đáp án B.
Bảo toàn khối lượng:
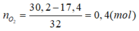
=> V = 0,4.22,4 = 8,96 (lít)

Bảo toàn khối lượng: m oxi = 30 , 2 – 17 , 4 = 12 , 8 → n oxi = 0 , 4 mol
→ V = 0,4.22,4 = 8,96 lít.
Chọn đáp án B.

Đáp án : D
Bảo toàn khối lượng => mO2 phản ứng = 30,2 – 17,4 = 12,8g
=> nO2 = 0,4 mol => V = 8,96lit
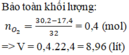

$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
$2Mg + O_2 \xrightarrow{t^o} 2MgO$
$m_Y = m_X + m_{O_2} = 17,4 + 12,8 = 30,2(gam)$