Đốt 8,9 hchc A cần dùng 0,375(mol) O2 thu được CO2, H2O,N2. Dẫn toàn bộ sản phẩm qua dd Ca(OH)2 dư thu được 0,3 mol kết tủa. Nếu đốt 6,675g A thì thu được 0,0374 mol N2.Hóa hơi 4,45g A thu được thể tích bằng thể tích của 0,8g khí CH4. Xác định CTPT của A?
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

26 tháng 5 2019
Chọn đáp án B.
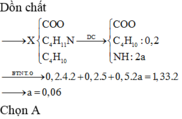
E là tetrapeptit nhưng lại phản ứng với NaOH tỉ lệ 1:6 => là đồng đẳng của axit glutamic
Đề bài không cho Ba(OH)2 dư nên chỉ tìm được mCO2 + mH2O = 41,37 – 18,81 = 22,56 gam
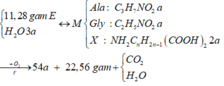
=>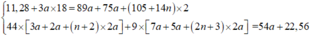
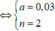
Vậy X là NH2CH(COOH)CH2COOH => Mx = 133 đvC.
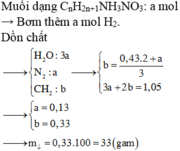

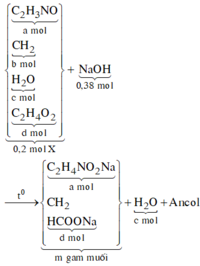
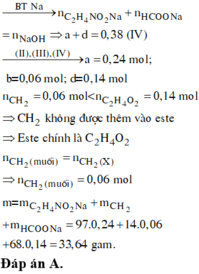

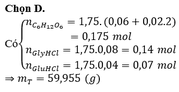

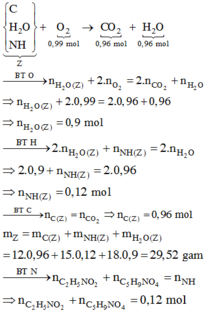



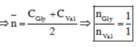
Sửa đề: 0,0374 (mol) N2 → 0,0375 (mol) N2
Ta có: \(n_{C\left(8,9\left(g\right)A\right)}=n_{CO_2}=n_{CaCO_3}=0,3\left(mol\right)\)
\(n_{N\left(6,675\left(g\right)A\right)}=2n_{N_2}=0,0375.2=0,075\left(mol\right)\)
\(\Rightarrow n_{N\left(8,9\left(g\right)A\right)}=\dfrac{0,075.8,9}{6,675}=0,1\left(mol\right)\) ⇒ nN2 (8,9 (g) A) = 0,05 (mol)
Theo ĐLBT KL, có: mA + mO2 = mCO2 + mH2O + mN2 (trong 8,9 (g) A)
⇒ mH2O = 8,9 + 0,375.32 - 0,3.44 - 0,05.28 = 6,3 (g)
\(\Rightarrow n_{H\left(8,9\left(g\right)A\right)}=2n_{H_2O}=2.\dfrac{6,3}{18}=0,7\left(mol\right)\)
Có: mC + mH + mN = 0,3.12 + 0,7.1 + 0,1.14 = 5,7 (g) < 8,9 (g)
→ A gồm các nguyên tố: C, H, O, N.
⇒ mO = 8,9 - 5,7 = 3,2 (g) ⇒ nO (8,9 (g) A) = 0,2 (mol)
Gọi CTPT của A là CxHyOzNt.
Có: x:y:z:t = 0,3:0,7:0,2:0,1 = 3:7:2:1
⇒ CTĐGN của A là (C3H7O2N)n
Ta có: \(n_{\left(4,45\left(g\right)A\right)}=\dfrac{0,8}{16}=0,05\left(mol\right)\) \(\Rightarrow M_A=\dfrac{4,45}{0,05}=89\left(g/mol\right)\)
\(\Rightarrow n=\dfrac{89}{12.3+7+16.2+14}=1\)
Vậy: CTPT của A là C3H7O2N.