Cho hỗn hợp A gồm Al và CuO phản ứng vừa hết với 36,5 gam acid HCl; sau phản ứng thấy thoát ra 7,437 lít khi ở đkc. Tỉnh % khối lượng mỗi chất trong hỗn hợp A.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) \(m_X=0,1\cdot64+0,2\cdot27+0,3\cdot24=19\left(g\right)\)
\(\Rightarrow\%m_{Cu}=\dfrac{0,1\cdot64\cdot100}{19}=34\%\)
\(\Rightarrow\%m_{Al}=\dfrac{0,2\cdot27\cdot100}{19}=28\%\)
\(\Rightarrow\%m_{Mg}=100\%-34\%-28\%=38\%\)
b) \(Cu+2HCl\rightarrow CuCl_2+H_2\) (1)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\) (2)
\(Mg+2HCl\rightarrow MgCl_2+H_2\) (3)
\(n_{HCl\left(1\right)}=2n_{Cu}=2\cdot0,1=0,2\left(mol\right)\)
\(n_{HCl\left(2\right)}=\dfrac{6\cdot n_{Al}}{2}=3\cdot0,2=0,6\left(mol\right)\)
\(n_{HCl\left(3\right)}=2n_{Mg}=2\cdot0,3=0,6\left(mol\right)\)
\(\Rightarrow m_{HCl}=\left(0,2+0,6+0,6\right)\cdot36,5=51,1\left(g\right)\)
\(n_{H_2\left(1\right)}=n_{Cu}=0,1\left(mol\right);n_{H_2\left(2\right)}=\dfrac{3\cdot0,2}{2}=0,3\left(mol\right);n_{H_2\left(3\right)}=n_{Mg}=0,3\left(mol\right)\)
\(V_{H_2\left(dkc\right)}=\left(0,1+0,3+0,3\right)\cdot24,79=17,353\left(l\right)\)

X +O2 → Y => Bảo toàn khối lượng => nO2 = 0,033 mol
Khi Y phản ứng với HCl thực chất là thay thế 1 mol O bằng 2 mol Cl theo bảo toàn điện tích
=> n HCl = 2n O = 4nO2 = 0,132 mol=>V= 0,132 l
=>B

Đáp án : C
Bảo toàn khối lượng :
mKL + m O 2 = mY
=> n O 2 = 0,045 mol
Tổng quát cả quá trình :
O + 2H -> H2O
=> nHCl = 4 n O 2 = 0,18 mol
=> Vdd HCl = 0,6 lit

\(n_{Al}=\dfrac{44,88-38,4}{27}=0,24\left(mol\right)\)
\(n_{CuO}=\dfrac{38,4}{80}=0,48\left(mol\right)\)
PTHH: 3CuO + 2Al --to--> 3Cu + Al2O3
Xét tỉ lệ: \(\dfrac{0,48}{3}>\dfrac{0,24}{2}\) => CuO dư, Al hết
PTHH: 3CuO + 2Al --to--> 3Cu + Al2O3
0,36<--0,24-------------->0,12
=> \(\left\{{}\begin{matrix}n_{Al_2O_3}=0,12\left(mol\right)\\n_{CuO\left(dư\right)}=0,12\left(mol\right)\end{matrix}\right.\)
PTHH: Al2O3 + 6HCl --> 2AlCl3 + 3H2O
0,12-->0,72
CuO + 2HCl --> CuCl2 + H2O
0,12-->0,24
=> nHCl = 0,72 + 0,24 = 0,96 (mol)

nHCl = 1 (mol)
Mg + 2HCl ---> MgCl2 + H2
Fe + 2HCl ---> FeCl2 + H2
2Al + 6HCl ---> 2AlCl3 + 3H2
Theo PTHH, ta thấy: \(n_{H_2}=\dfrac{1}{2}.n_{HCl}=\dfrac{1}{2}.1=0,5\left(mol\right)\)
\(\Rightarrow m_{H_2}=0,5.2=1\left(g\right)\)
Bảo toàn khối lượng => m = 13,4 + 36,5 - 1 = 48,9 (g)

Bảo toàn KL: \(m_{O_2}=m_Y-m_X=5,6-3,68=1,92(g)\)
\(\Rightarrow n_{O_2}=\dfrac{1,92}{32}=0,06(mol)\\ \Rightarrow n_{O(O_2)}=0,12(mol)\\ \Rightarrow n_{oxit}=n_{O(O_2)}=0,012(mol)\\ \Rightarrow n_{H^+}=n_{HCl}=2n_{O(oxit)}=0,24(mol)\\ \Rightarrow V=\dfrac{0,24}{0,5}=0,48(l)\)
Chọn B

*Xét giai đoạn Y tác dụng với dung dịch NaOH:
Số mol NaOH là: ![]()
Sơ đồ phản ứng:
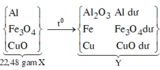
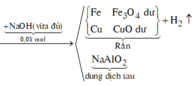
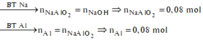
*Xét giai đoạn Y tác dụng với dung dịch HCl dư
Số mol H2 thu được là: ![]()
Chất rắn Z là Cu ![]()
Chất rắn Z là Cu => Dung dịch sau không chứa F e 3 +
Sơ đồ phản ứng:
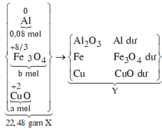
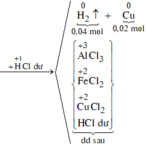
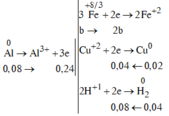
![]() => b = 0,06 mol
=> b = 0,06 mol
![]()
![]()
![]()
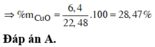

a)
\(Zn + 2HCl \to ZnCl_2 + H_2\\ Fe_2O_3 + 6HCl \to 2FeCl_3 + 3H_2\)
Theo PTHH : \(n_{Zn} = n_{H_2} = \dfrac{6,72}{22,4} = 0,3(mol)\)
\(\Rightarrow n_{Fe_2O_3} = \dfrac{35,5-0,3.65}{160} = 0,1\\ \Rightarrow n_{HCl} = 2n_{Zn} + 6n_{Fe_2O_3} = 0,3.2 + 0,1.6 = 1,2(mol)\\ \Rightarrow m_{HCl} = 1,2.36,5 = 43,8(gam)\)
b)
\(CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O\)
Gọi \(n_{CuO} = a;n_{Fe_2O_3} = b\)
\(\left\{{}\begin{matrix}80a+160b=19,6\\a+3b=0,3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,135\\b=0,055\end{matrix}\right.\)
Vậy :
\(\left\{{}\begin{matrix}n_{Cu}=0,135\\n_{Fe}=0,055.2=0,11\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}m_{Cu}=0,135.64=8,64\left(gam\right)\\m_{Fe}=0,11.56=6,16\left(gam\right)\end{matrix}\right.\)

Đáp án B
Khi phản ứng với Cl2
n C l 2 = 7 , 84 22 , 4 = 0 , 35 ( m o l )
X – ne → X +n Cl2+ 2e→ 2Cl-
ne (KL nhường) = ne ( Cl2 nhận ) = 0,35.2 = 0,7 (mol)
Khi phản ứng với HCl
X – ne → X +n 2H+ + 2e → H2
ne( H+ nhận ) = ne (KL nhường) = 0,7 (mol)
=> nH+ = 0,7 (mol)
=> mHCl = 0,7.36,5 = 25,55 (g)
m d d H C l = m H C l . 100 % C % = 25 , 55 . 100 % 14 , 6 % = 175 ( g )
PTHH:
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\) (1)
\(CuO+2HCl\rightarrow CuCl_2+H_2O\) (2)
\(n_{HCl\left(1\right)+\left(2\right)}=\dfrac{36,5}{36,5}=1\left(mol\right)\)
\(n_{H_2}=\dfrac{7,437}{24,79}0,3\left(mol\right)\)
Theo PTHH (1): \(n_{Al}=\dfrac{2\cdot0,3}{3}=0,2\left(mol\right)\); \(n_{HCl\left(1\right)}=\dfrac{6\cdot0,3}{3}=0,6\left(mol\right)\)
\(\Rightarrow m_{Al}=0,2\cdot27=5,4\left(g\right)\)
\(\Rightarrow n_{HCl\left(2\right)}=1-0,6=0,4\left(mol\right)\)
Theo PTHH (2): \(n_{CuO}=\dfrac{1\cdot0,4}{2}=0,2\left(mol\right)\)
\(\Rightarrow m_{CuO}=0,2\cdot80=16\left(g\right)\)
\(\Rightarrow m_A=m_{CuO}+m_{Al}=16+5,4=21,4\left(g\right)\)
% khối lượng của mỗi chất trong hỗn hợp A là:
\(\%m_{Al}=\dfrac{5,4\cdot100}{21,4}\approx25,2\%\)
\(\Rightarrow\%m_{CuO}=100\%-25,2\%=74,8\%\)