Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)

\(n_{FeO}=a\left(mol\right),n_{CuO}=b\left(mol\right)\)
\(m_{hh}=72a+80b=19.2\left(g\right)\left(1\right)\)
\(FeO+H_2SO_4\rightarrow FeSO_4+H_2O\)
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
\(n_{H_2SO_4}=a+b=0.25\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.15\)
\(m_{FeO}=0.1\cdot72=7.2\left(g\right)\)
\(m_{CuO}=12\left(g\right)\)
\(C_{M_{FeSO_4}}=\dfrac{0.1}{0.25}=0.4\left(M\right)\)
\(C_{M_{CuSO_4}}=\dfrac{0.15}{0.25}=0.6\left(M\right)\)

m rắn giảm = mO (oxit) => nO (oxit) = (1,6 – 1,408) : 16 = 0,012mol
Dễ thấy n = nO (oxit) = 0,012mol
=> nH2 ban đầu = 0,012 : 80% = 0,015
=> nFe = nH2= 0,015 → x = 0,015
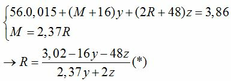
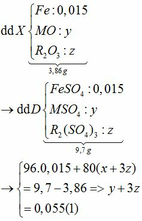
Ta có: CO + O(Oxit) → CO2
Vì: m(Rắn giảm) = mO(Oxit) → nO(Oxit) = (3,86 – 3,46) : 16 = 0,025
TH1: cả 2 oxit đều bị khử bởi CO
→ nO(Oxit) = y + 3z = 0,025 kết hợp với (1) loại
TH2: chỉ có MO bị khử bởi CO
→ nO(Oxit) = nMO = 0,025 → y = 0,025 kết hợp với (1) => z = 0,01
Kết hợp với (*) => M = 64 (Cu)
TH3: chỉ có R2O3 bị khử bởi CO
→ nO(Oxit) = 3.nR2O3 → z = 0,025/3 kết hợp với (1) => y = 0,03
Kết hợp với (*) y => M lẻ => loại
Vậy %m các chất trong X là: 21,76%; 51,81%; 26,43%

Zn+ H2SO4→ ZnSO4+ H2↑
(mol) 0,1 0,1 0,1
a)
\(n_{H_2}=\dfrac{V}{22,4}=\dfrac{2,24}{22,4}=0,1\left(lít\right)\)
→mZn=n.M=0,1.65= 6,5(g)
→mCu= 10- 6,5= 3,5(g)
=> \(\%m_{Zn}=\dfrac{6,5}{10}.100\%=65\%\)
\(\%m_{Cu}=100\%-65\%=35\%\)
b) \(C_{M_{H_2SO_4}}=\dfrac{n}{V}=\dfrac{0,1}{0,1}=1M\)

a) \(n_{CuO}=\dfrac{2,4}{80}=0,03\left(mol\right)\)
\(m_{H_2SO_4}=100.29,4\%=29,4\left(g\right)\Rightarrow n_{H_2SO_4}=\dfrac{29,4}{98}=0,3\left(mol\right)\)
PTHH: CuO + H2SO4 → CuSO4 + H2O
Mol: 0,03 0,03 0,03
Ta có: \(\dfrac{0,03}{1}< \dfrac{0,3}{1}\) ⇒ CuO hết, H2SO4 dư
b) \(m_{H_2SO_4}=0,03.98=2,94\left(g\right)\)
c) mdd sau pứ = 2,4+100 = 102,4 (g)
\(C\%_{ddCuSO_4}=\dfrac{0,03.160.100\%}{102,4}=4,6875\%\)
\(C\%_{ddH_2SO_4dư}=\dfrac{\left(0,3-0,03\right).98.100\%}{102,4}=25,84\%\)
Bài 4 :
\(n_{CuO}=\dfrac{2,4}{80}=0,03\left(mol\right)\)
\(m_{ct}=\dfrac{29,4.100}{100}=29,4\left(g\right)\)
\(n_{H2SO4}=\dfrac{29,4}{98}=0,3\left(mol\right)\)
a) Pt : \(CuO+H_2SO_4\rightarrow CuSO_4+H_2O|\)
1 1 1 1
0,03 0,3 0,03
Câu khối lượng của dng dịch H2SO4 đề cho rồi nên mình làm câu c thôi nhé
c) Lập tỉ số so sánh : \(\dfrac{0,03}{1}< \dfrac{0,3}{1}\)
⇒ CuO phản ứng hết , H2SO4 dư
⇒ Tính toán dựa vào số mol của CuO
\(n_{CuSO4}=\dfrac{0,03.1}{1}=0,03\left(mol\right)\)
⇒ \(m_{CuSO4}=0,03.160=4,8\left(g\right)\)
\(n_{H2SO4\left(dư\right)}=0,3-0,03=0,27\left(mol\right)\)
⇒ \(m_{H2SO4\left(dư\right)}=0,27.98=26,46\left(g\right)\)
\(m_{ddspu}=2,4+100=102,4\left(g\right)\)
\(C_{CuSO4}=\dfrac{4,8.100}{102,4}=4,6875\)0/0
\(C_{H2SO4\left(dư\right)}=\dfrac{26,46.100}{102,4}=25,84\)0/0
Chúc bạn học tốt

Câu 1
mCaCO3 = 90*15/100 = 13,5 tấn
PT: CaCO3 ➙ CaO + CO2
100g 56g
13,5tấn 7,56tấn
mCaO = 7,56*85/100 = 6,426 tấn

a) \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
____0,15<--0,3<--------------0,15
=> mFe = 0,15.56 = 8,4 (g)
=> \(\left\{{}\begin{matrix}\%Fe=\dfrac{8,4}{21,2}.100\%=39,62\%\\\%Cu=\dfrac{21,2-8,4}{21,2}.100\%=60,38\%\end{matrix}\right.\)
b) mHCl = 0,3.36,5 = 10,95(g)
=> \(m_{ddHCl}=\dfrac{10,95.100}{3,65}.100\%=300\left(g\right)\)

a) Đặt số mol của MO, M(OH)2, MCO3 tương ứng là x, y, z.
Nếu tạo muối trung hòa ta có các phản ứng:
MO + H2SO4 →MSO4 + H2O (1)
M(OH)2 + H2SO4 →MSO4 + 2H2O (2)
MCO3 + H2SO4 →MSO4 + H2O + CO2 (3)
Nếu tạo muối axít ta có các phản ứng:
MO + 2H2SO4 →M(HSO4)2 + H2O (4)
M(OH)2 + 2H2SO4 →M(HSO4)2 + 2H2O (5)
MCO3 + 2H2SO4 →M(HSO4)2 + H2O + CO2 (6)
Ta có :
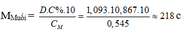
– TH1: Nếu muối là MSO4 M + 96 = 218 M = 122 (loại)
– TH2: Nếu là muối M(HSO4)2 M + 97.2 = 218 M = 24 (Mg)
Vậy xảy ra phản ứng (4, 5, 6) tạo muối Mg(HSO4)2
b) Theo (4, 5, 6) Số mol CO2 = 0,448/22,4 = 0,02 molz = 0,02 (I)
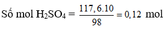
2x + 2y + 2z = 0,12 (II)
Đề bài: 40x + 58y + 84z = 3,64 (III)
Giải hệ (I, II, III): x = 0,02; y = 0,02; z = 0,02
%MgO = 40.0,02.100/3,64 = 21,98%
%Mg(OH)2 = 58.0,02.100/3,64 = 31,87%
%MgCO3 = 84.0,02.100/3,64 = 46,15%

a)
Chất rắn sau phản ứng là Cu
$Fe + H_2SO_4 \to FeSO_4 + H_2$
$n_{Fe} = n_{H_2} = \dfrac{1,12}{22,4} = 0,05(mol)$
$m_{Fe} = 0,05.56 = 2,8(gam)$
$\Rightarrow m_{Cu} = 10,5 - 2,8 = 7,7(gam)$
b) $n_{H_2SO_4} = n_{H_2} = 0,05(mol)$
$\Rightarrow m_{H_2SO_4} = 0,05.98 = 4,9(gam)$