Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: 2KOH+KH2PO4--->K3PO4+2H2O
Hoặc: KOH(loãng)+KH2PO4---> K2HPO4+H2O
KOH(đậm đặc)+K2HPO4---> K3PO4+H2O
2KOH + KH2PO4 -> K3PO4 + 2H2O
KOH + K2HPO4 ko xảy ra thì phải

KOH+KH2PO4->K2HPO4+H2O(1)
K2HPO4+KOH->K3PO4+H2O(2)
Từ (1)->nK2HPO4=nKH2PO4=0.3mol
->nK2HPO4=0.3+0.1=0.4mol
nKOH dư sau (1)=150x22.4%:56-0.3=0.3mol
nKOH dư<nK2HPO4
->(2)xảy ra không hoàn toàn
->Sản phẩm gồm K2HPO4 và K3PO4

a) \(n_{NaOH}=0,2.1=0,2\left(mol\right);n_{H_2SO_4}=0,15.2=0,3\left(mol\right)\)
PTHH: 2NaOH + H2SO4 → Na2SO4 + 2H2O
Mol: 0,2 0,1
Ta có: \(\dfrac{0,2}{2}< \dfrac{0,3}{1}\) ⇒ NaOH hết, H2SO4 dư
\(m_{Na_2SO_4}=0,1.142=14,2\left(g\right)\)
b) Vdd sau pứ = 0,2 + 0,15 = 0,35 (l)
\(C_{M_{ddNa_2SO_4}}=\dfrac{0,1}{0,35}=\dfrac{2}{7}\approx0,2857M\)
\(C_{M_{ddH_2SO_4dư}}=\dfrac{0,3-0,1}{0,35}=\dfrac{4}{7}\approx0,57M\)

9
nSO2 = 4,48 : 22,4 = 0,2 (mol) ; nNaOH = 16: 40 = 0,4 (mol)
Ta thấy nNaOH/ nSO2 = 2 => chỉ tạo muối Na2SO3
=> mNa2SO3 = 0,2. 126 = 25, 2(g) =>D
10
nBa(OH) = 0,15.1 = 0,15mol; nBaCO3 = 19,7 : 197 = 0,1mol
Vì nBaCO3 < nBa(OH)2 → xét 2 trường hợp
Trường hợp 1: Ba(OH)2 dư, CO2 hết, phản ứng chỉ tạo muối cacbonat
CO2 + Ba(OH)2 → BaCO3 + H2O
0,1 0,1
Vậy V = VCO2 = 0,1.22,4 =2,24
Trường hợp 2: Phản ứng sinh ra 2 muối cacbonat và hiđrocacbonat
CO2 + Ba(OH)2→ BaCO3 + H2O (1)
0,1 0,1 0,1
2CO2+Ba(OH)2→Ba(HCO3)2
0,1 0,05
Theo phương trình (1): nBa(OH)2(1) = nBaCO3=0,1mol
Mà nBa(OH)2= 0,15mol →nBa(OH)2 (2) = 0,15−0,1 = 0,05mol
Theo (1) và (2): nCO2 = nBaCO3 + 2nBa(OH)2 (2) = 0,1 + 2.0,05 = 0,2 mol
Vậy V = VCO2 = 0,2.22,4 = 4,48 lít
=>A

a/nBa(OH)2)=0,3 mol
nHCl=0,18 mol
PTHH: Ba(OH)2 +2 HCl _>BaCl2 + H2O
bđ: 0,3 0,18 0 mol
pư: 0,09 0,18 0,09 mol
sau pứ: 0,21 0 0,09 mol
sau phản ứng Ba(OH)2 dư 0,21 mol nên làm q tím chuyển sang màu XANH
b/ nCO2 = 0,3 mol
khúc sau mình khong bk

\(n_{CuCl_2}=2.0,2=0,4(mol)\\ n_{NaOH}=2.0,2=0,4(mol)\\ a,CuCl_2+2NaOH\to Cu(OH)_2+2NaCl\\ Cu(OH)_2\xrightarrow{t^o}CuO+H_2O\\ b,\dfrac{n_{CuCl_2}}{1}>\dfrac{n_{NaOH}}{2}\Rightarrow CuCl_2\text{ dư}\\ \Rightarrow n_{CuO}=0,2(mol)\\ \Rightarrow m_{CuO}=0,2.80=16(g)\\ c,n_{CuCl_2(dư)}=0,4-0,2=0,2(mol)\\n_{NaCl}=0,2(mol)\\ \Rightarrow m_{CuCl_2(dư)}=0,2.135=27(g)\\ m_{NaCl}=0,2.58,5=11,7(g)\)

n H3PO4 = 2,94/98 = 0,03(mol)
n KOH = 4,2/56 = 0,075(mol)
Ta có :
2< n KOH / n H3PO4 = 0,075/0,03 = 2,5 < 3
Do đó tạo thành K2HPO4(a mol) ; K3PO4(b mol)
Bảo toàn nguyên tố với K, P
n KOH = 2a + 3b = 0,075
n H3PO4 = a + b = 0,03
=> a = b = 0,015
Vậy :
m K2HPO4 = 0,015.174 = 2,61 gam
m K3PO4 = 0,015.212 = 3,18(gam)

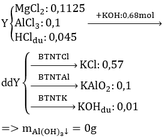
Bạn xem lại đề có chính xác hay chưa nhé!
Bài 6 đấy ak