
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.





Chọn A.
Gọi thành phần phần trăm hai đồng vị lần lượt là a,b.
Ta có: \(\left\{{}\begin{matrix}a+b=100\%\\35a+37b=35,5\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=75\%\\b=25\%\end{matrix}\right.\)
Khi đó \(\%^{35}Cl=75\%\)
\(\overline{M_{FeCl_3}}=55,85+3\cdot35,5=162,35\)
\(\%^{35}Cl_{\left(trongFeCl_3\right)}=\dfrac{75\%\cdot35,5}{162,35}\approx16,4\%\)



\(a) n_{CO_2} = a(mol) ; n_{H_2} = b(mol)\\ n_A = \dfrac{6,72}{22,4} = 0,3(mol)\)
Ta có :
a + b = 0,3
44a + 2b = 0,3.2.15
Suy ra a = 0,2 ; b = 0,1
\(Mg + H_2SO_4 \to MgSO_4 + H_2\\ FeCO_3 + H_2SO_4 \to FeSO_4 + CO_2 + H_2O\\ \)
n Mg = n H2 = 0,1(mol)
n FeCO3 = n CO2 = 0,2(mol)
\(\%m_{Mg} = \dfrac{0,1.24}{0,1.24 + 0,2.116}.100\% = 9,375\%\\ \%m_{FeCO_3} = 100\%-9,375\% = 90,625\%\)
b)
Bảo toàn nguyên tố C : n CO2 = n FeCO3 = 0,2(mol)
Bảo toàn e : 2n SO2 = 2n Mg + n FeCO3
=> n SO2 = (0,1.2 + 0,2)/2 = 0,2(mol)
=> V khí = (0,2 + 0,2).22,4 = 8,96 lít

Câu 1 :
a) $Cu + 2H_2SO_4 \to CuSO_4 + SO_2 + 2H_2O$
b) SO2 là khí không màu ,mùi sốc,nặng hơn không khí, tan nhiều trong nước.
c) n Cu = n SO2 = 6,72/22,4 = 0,3(mol)
m Cu = 0,3.64 = 19,2(gam)
m Fe = 28,9 - 19,2 = 9,7(gam)
d)
%m Cu = 19,2/28,9 .100% = 66,44%
%m Fe = 100% -66,44% = 33,56%
Câu 2 :
a) $Zn + 2H_2SO_4 \to ZnSO_4 + SO_2 + H_2O$
b) SO2 là khí không màu ,mùi sốc,nặng hơn không khí, tan nhiều trong nước
c) n Zn = n SO2 = 8,96/22,4 = 0,4(mol)
m Zn = 0,4.65 = 26(gam)
m Al = 30,5 -26 = 4,5(gam)
d)
%m Zn = 26/30,5 .100% = 85,25%
%m Al = 100%- 85,25% = 14,75%
Câu 3 :
Tác dụng với H2SO4 loãng : Fe,CuO,FeS
$Fe + H_2SO_4 \to FeSO_4 + H_2$
$CuO + H_2SO_4 \to CuSO_4 + H_2O$
$FeS + H_2SO_4 \to FeSO_4 + H_2S$
Tác dụng với H2SO4 đặc : Fe,Cu,CuO,FeS
$2Fe + 6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O$
$Cu + 2H_2SO_4 \to CuSO_4 + SO_2 + 2H_2O$
$2FeS + 10H_2SO_4 \to Fe_2(SO_4)_3 + 9SO_2 + 10H_2O$
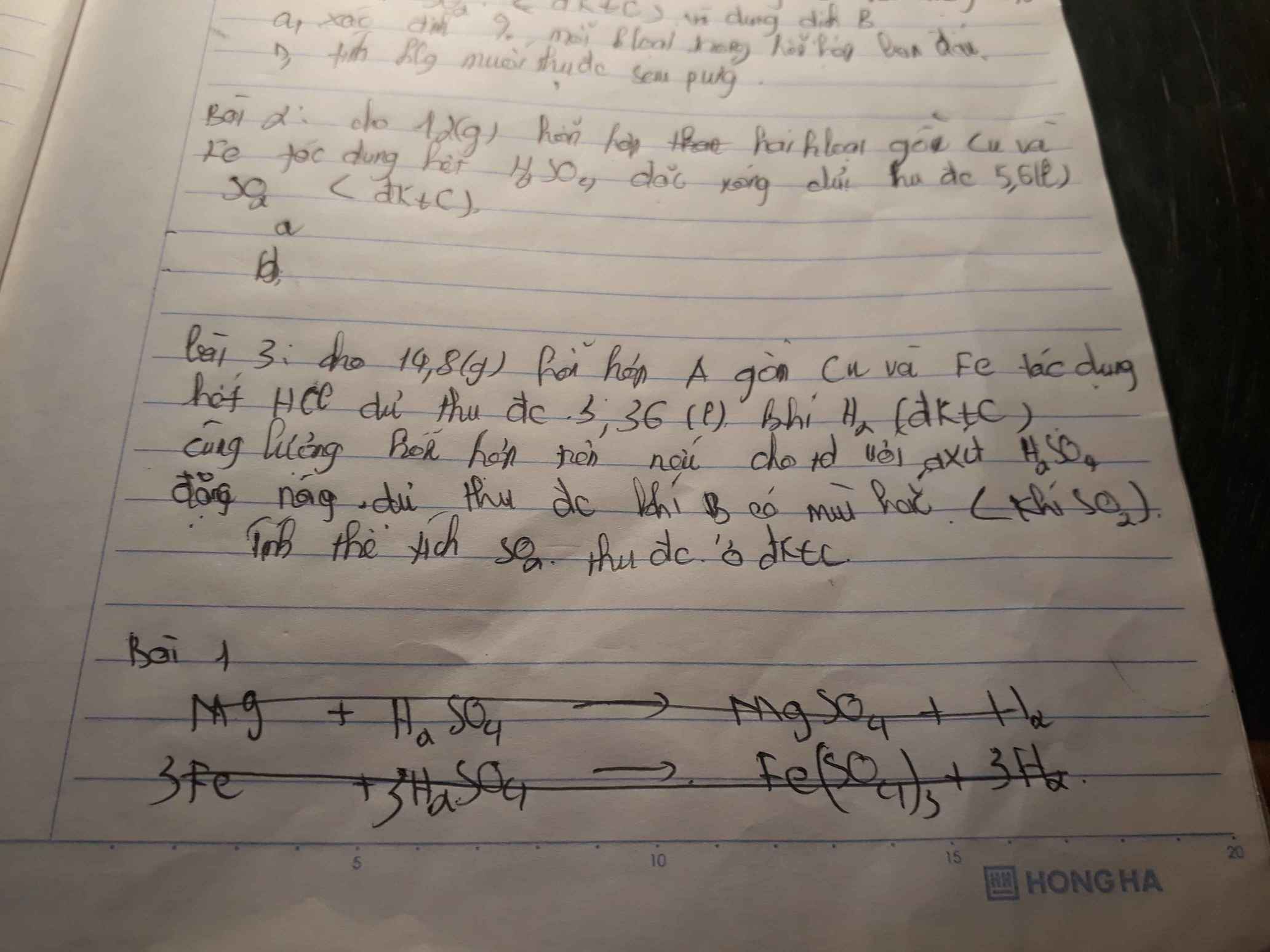






Bài 3 :
\(Fe + 2HCl \to FeCl_2 + H_2\\ n_{Fe} = n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)\\ \Rightarrow n_{Fe} = \dfrac{14,8-0,15.56}{64} = 0,1(mol)\\ Fe^0 \to Fe^{+3} + 3e\\ Cu^{0} \to Cu^{+2} + 2e\\ S^{+6} + 2e \to S^{+4}\\ n_{SO_2} = \dfrac{3n_{Fe} + 2n_{Cu}}{2} = 0,325(mol)\\ V_{SO_2} = 0,325.22,4 = 7,28(lít)\)