Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
2Al + 6HCl → 2AlCl3 + 3H2↑
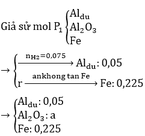
Pt: 2Al + 6H2SO4 → Al2(SO4)3 + 3SO2↑ + 6H2O
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ + 6H2O
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Giả sử P2 = kP1
=> a=0.1
=> m = 128,8g
b)
2yAl + 3FexOy → yAl2O3 + 3xFe
0,1 0,225
=> 0,225y = 0,3x => 3y = 4x
=> Fe3O4

Phần 2: nCO32- phản ứng = u và nHCO3- phản ứng = v
nCO2 = u + v = 0,06
nHCl = 2u + v = 0,075
—> u = 0,015 và v = 0,045
—> Phần 1: nCO32- = ku và nHCO3- = kv
—> nCaCO3 = ku + kv = 0,1
—> k = 5/3
Vậy X chứa nCO32- = 2ku = 0,05 và nHCO3- = 2kv = 0,15
Bảo toàn điện tích —> nNa+ = x + 2y = 0,05.2 + 0,15
Bảo toàn C —> 0,1 + y = 0,05 + 0,15
—> x = 0,05 và y = 0,1
nhớ tick nếu thấy đúng nha

Theo gt ta có: $n_{CO_2}=0,1(mol);n_{CaCO_3}=0,1(mol);n_{HCl}=0,075(mol);n_{CO_2/(2)}=0,06(mol)$
Bảo toàn C ta có: $y=0,1$
$CO_3^{2-}+2H^+\rightarrow CO_2+H_2O$
$HCO_3^-+H^+\rightarrow CO_2+H_2O$
Gọi số mol $CO_3^{2-}$ và $HCO_3^-$ phản ứng lần lượt là a;b
Ta có: $2a+b=0,075;a+b=0,06$
Giải hệ ta được $a=0,015;b=0,045$
Suy ra $n_{CO_3^{2-}}=0,05(mol);n_{HCO_3}=0,15(mol)$
Bảo toàn Na ta có: $x=0,05$

Tính toán theo PTHH :
Fe3O4 + 8 HCl → 2 FeCl3 + FeCl2 + 4 H2O
FeCl2 + ½ Cl2 → FeCl3
FeCl2 + 3 AgNO3 → 2 AgCl + Ag + Fe(NO3)3
FeCl3 + 3 AgNO3 → 3 AgCl + Fe(NO3)3
Bảo toàn khối lượng
m2 – 0,5 m1 = m Cl2 ( lưu ý hỗn hợp chia làm 2 phần nên muối phản ứng ở mỗi phần là 0,5 m1 )
m2 – 0,5 m1 = m Cl2 => m Cl2 = 1,42 => n Cl2 = 0,02 mol
Theo PTHH : n FeCl2 = n Cl2 . 2 = 0,04 mol
Theo PTHH : n FeCl2 . 2 = n FeCl3 = 0,08 mol
Theo PTHH : n AgCl = 2 . nFeCl2 + 3 . n FeCl3 = 0,08 .3 + 0,04 .2 = 0,32 mol
n Ag = n FeCl2 = 0,04 mol
=> m Chất rắn = m Ag + m AgCl = 0,04 . 108 + 0,32 . 143,5 = 50,24 g
phản ứng của Fe2+ + Ag+ → Fe+3 + Ag

mdd giảm = m↓ - mCO2 → mCO2 = 10 - 3,4 = 6,6 gam → nCO2 = 6,6 : 44 = 0,15 mol.
C6H12O6 enzim−−−−→30−35oC→30-35oCenzim2C2H5OH + 2CO2
Theo phương trình: nC6H12O6 = 0,15 : 2 = 0,075 mol.
Mà H = 90% → nC6H12O6 = 0,075 : 90% = 1/12 mol → m = 180 x 1/12 = 15 gam


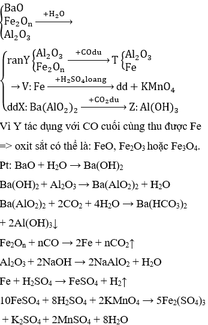
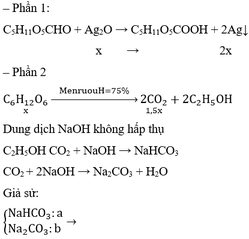

chắc còn đấy,làm đi
Cần nha=)))) đề Tuyển sinh mà hong cần