Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{CO}=a\left(mol\right),n_{CO_2}=b\left(mol\right)\)
\(n_B=a+b=0.5\left(mol\right)\)
\(m_B=20.4\cdot2\cdot0.5=20.4\left(g\right)\)
\(\Leftrightarrow28a+44b=20.4\)
\(KĐ:a=0.1,b=0.4\)
\(n_{CO\left(pư\right)}=n_{CO_2}=0.4\left(mol\right)\)
\(BTKL:\)
\(m=0.4\cdot44+64-0.4\cdot28=70.4\left(g\right)\)

A, Gọi X,y lần lượt là số mol của Mg và Al
Pthh:
Mg + H2SO4---> MgSO4 + H2
X. X. X. X
2Al + 3H2SO4---> Al2(SO4)3+3H2
Y. 1.5y. Y. 1.5y
Ta có pt:
24x + 27y= 1.95
X+1.5y=2.24/22.4=0.1
=> X=0.025, Y=0.05
%Mg= 0.025×24×100)/1.95=30.8%
%Al= 100%-30.8%=69.2%
mH2SO4= 0.025+1.5×0.05=0.1g
mH2= (0.025+0.05)×2=0.15g
C, Mdd H2SO4 = 0.1/6.5×100=1.54g
MddY= 1.54+1.95-0.15=3.34g
%MgSO4 vs %Al2(SO4)3 b tự tính nha

Dung dịch Ca(OH)2 không hấp thụ khí CO nên 6,72 lít khí thoát ra chính là khí CO dư.


Các phản ứng khử sắt oxit có thể có:
3Fe2O3 + CO ---> 2Fe3O4 + CO2 (1)
Fe3O4 + CO ---->3FeO + CO2 (2)
FeO + CO ---> Fe + CO2 (3)
Như vậy chất rắn A có thể gồm 3 chất Fe, FeO, Fe3O4 hoặc ít hơn, điều đó không quan trọng và việc cân bằng các phương trình trên cũng không cần thiết, quan trọng là số mol CO phản ứng bao giờ cũng bằng số mol CO2 tạo thành.
mol.
Gọi x là số mol của CO2 ta có phương trình về khối lượng của B:
44x + 28(0,5 - x) = 0,5 * 20,4 * 2 = 20,4
nhận được x = 0,4 mol và đó cũng chính là số mol CO tham gia phản ứng.
Theo ĐLBTKL ta có:
mX + mCO = mA +
m = 64 + 0,4* 44 - 0,4 * 28 = 70,4 gam.

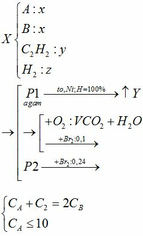
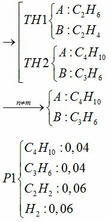
CO tác dụng với hỗn hợp oxit dư thu được khí X là C O 2 .
C O 2 tác dụng với C a O H 2 dư thu được muối duy nhất là kết tủa C a C O 3
⇒ n C O 2 = n N a C O 3 = 4/100 = 0,04 mol
⇒ nCO = n C O 2 = 0,04 mol
⇒ VCO = 0,04.224 = 0,896 lit
⇒ Chọn A.

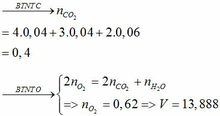

\(n_{CO\left(bđ\right)}=\dfrac{5.6}{22.4}=0.25\left(mol\right)\)
\(CO+O_{oxit}\rightarrow CO_2\)
\(n_{CO}=n_Y=0.25\left(mol\right)\)
\(M_Y=18.8\cdot2=37.6\left(\dfrac{g}{mol}\right)\)
Bảo toàn khối lượng :
\(m_A=37.6\cdot0.25+12.32-0.25\cdot28=14.72\left(g\right)\)
cảm ơn ạ